第1课时二氧化硫的性质和作用[核心素养发展目标]1
会依据酸性氧化物的通性及硫元素的化合价分析理解二氧化硫的性质;知道二氧化硫具有漂白性
通过认识二氧化硫对空气的污染、酸雨的危害,增强环保意识
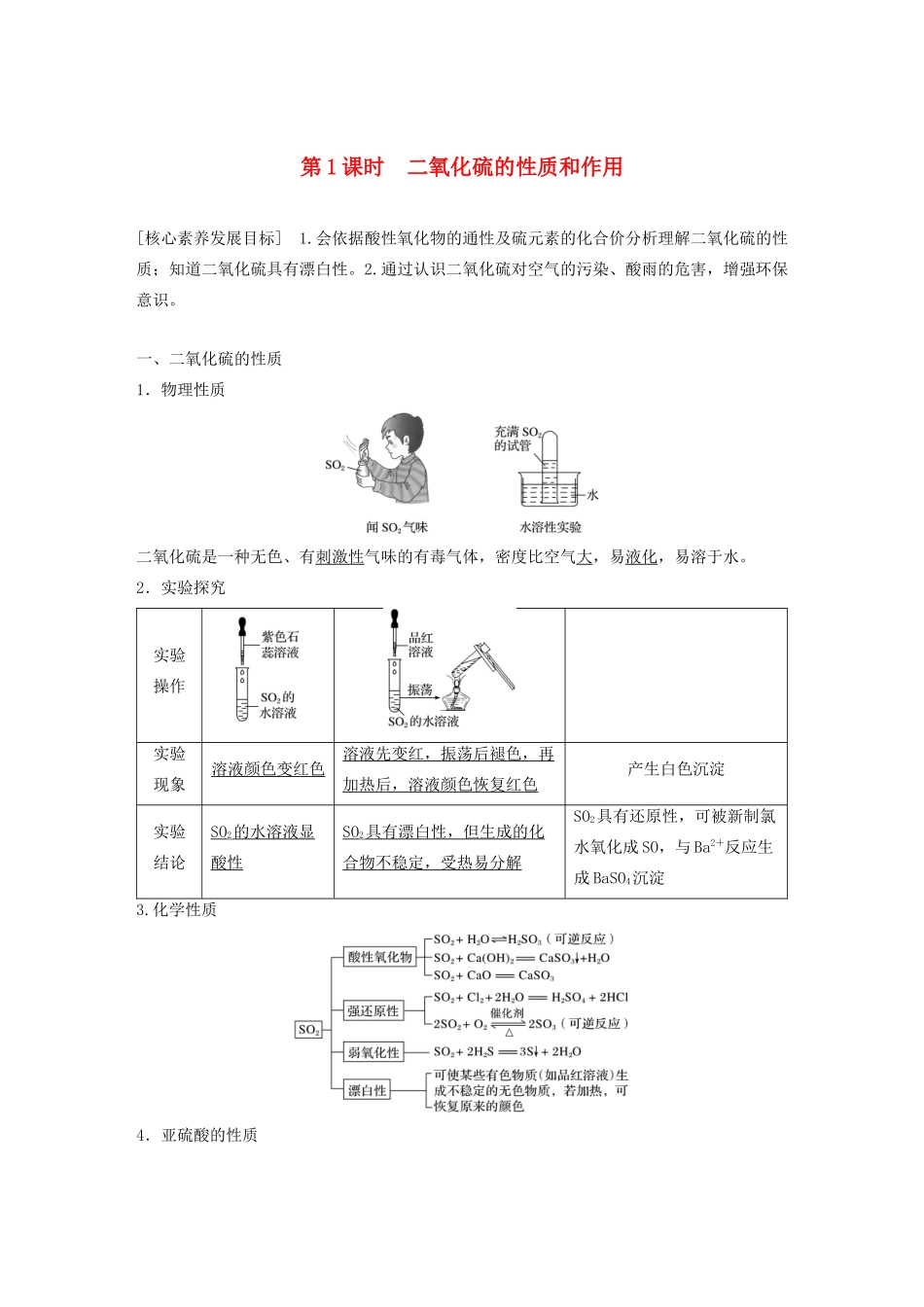
一、二氧化硫的性质1.物理性质二氧化硫是一种无色、有刺激性气味的有毒气体,密度比空气大,易液化,易溶于水
2.实验探究实验操作实验现象溶液颜色变红色溶液先变红,振荡后褪色,再加热后,溶液颜色恢复红色产生白色沉淀实验结论SO2的水溶液显酸性SO2具有漂白性,但生成的化合物不稳定,受热易分解SO2具有还原性,可被新制氯水氧化成SO,与Ba2+反应生成BaSO4沉淀3
化学性质4.亚硫酸的性质(1)二氧化硫与氯气的漂白性比较(2)可逆反应的含义可逆反应是在相同条件下,既能向正反应方向进行,同时又能向逆反应方向进行的反应
例1如图是研究二氧化硫性质的微型实验装置
现用60%硫酸溶液和亚硫酸钠晶体反应制取SO2气体,实验现象很明显,且不易污染空气
下列说法中错误的是()A.紫色石蕊溶液变蓝色B.品红溶液褪色C.溴水橙色褪去D.含酚酞的NaOH溶液红色变浅答案A解析SO2气体与水反应生成H2SO3,紫色石蕊溶液遇酸变红色,不会变蓝色,故A错误
例2下列说法正确的是()A.因为SO2具有漂白性,所以它能使品红溶液、溴水、KMnO4(H+)、石蕊溶液褪色B.能使品红溶液褪色的不一定是SO2C.SO2、漂白粉、活性炭、Na2O2都能使红墨水褪色,其原理相同D.等物质的量的SO2和Cl2相遇在溶液中具有漂白能力答案B解析SO2使溴水、酸性KMnO4溶液褪色是因为SO2具有还原性,能使品红褪色是因其漂白性,SO2不能使指示剂褪色,A项错误;因为能使品红褪色的物质很多,不仅仅是SO2,B项正确;因为这些漂白剂的漂白原理不相同,SO2漂白属于化合型,活性炭属于吸附型,漂白粉、Na2O2属于氧化型,C项错误