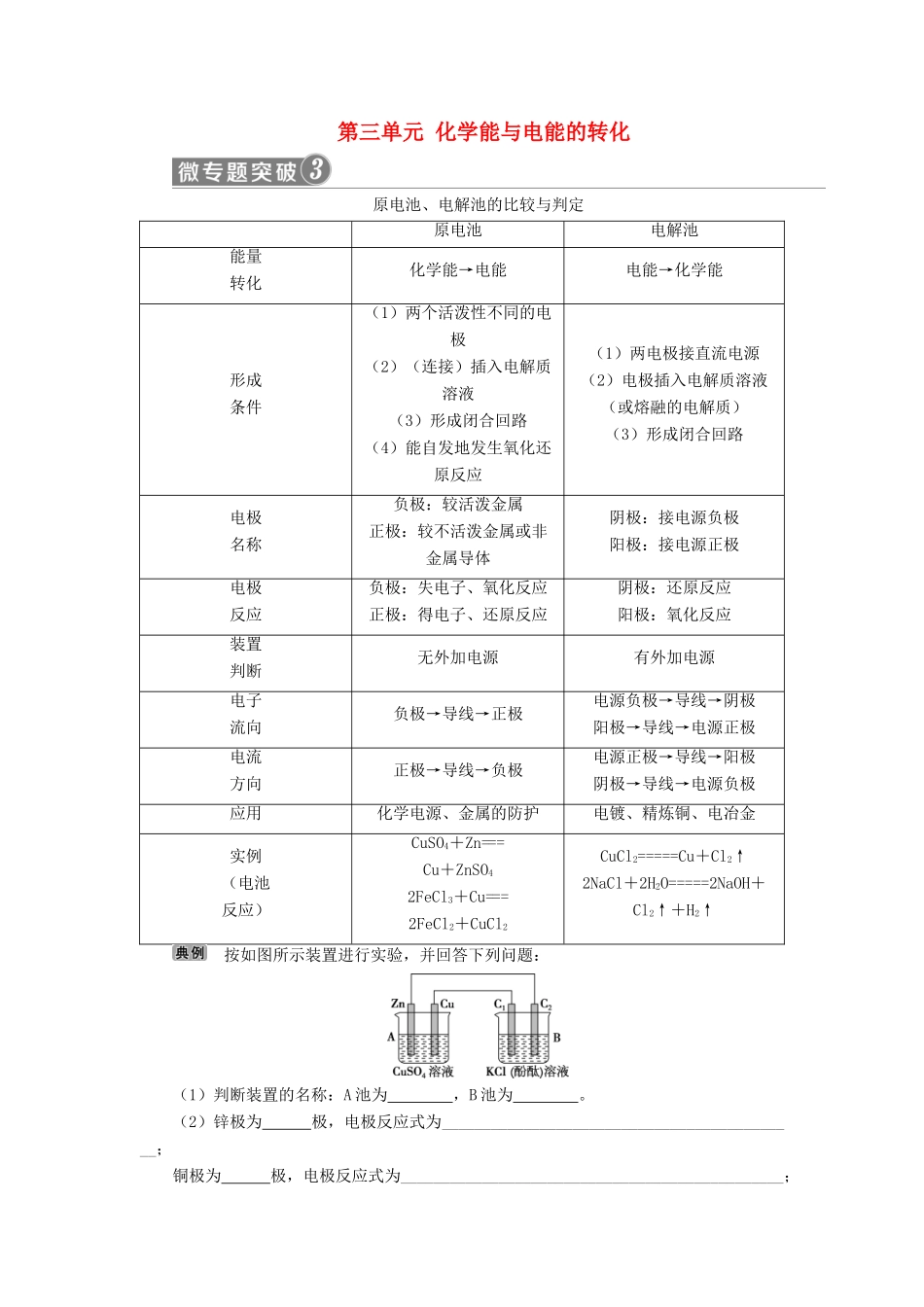
第三单元化学能与电能的转化原电池、电解池的比较与判定原电池电解池能量转化化学能→电能电能→化学能形成条件(1)两个活泼性不同的电极(2)(连接)插入电解质溶液(3)形成闭合回路(4)能自发地发生氧化还原反应(1)两电极接直流电源(2)电极插入电解质溶液(或熔融的电解质)(3)形成闭合回路电极名称负极:较活泼金属正极:较不活泼金属或非金属导体阴极:接电源负极阳极:接电源正极电极反应负极:失电子、氧化反应正极:得电子、还原反应阴极:还原反应阳极:氧化反应装置判断无外加电源有外加电源电子流向负极→导线→正极电源负极→导线→阴极阳极→导线→电源正极电流方向正极→导线→负极电源正极→导线→阳极阴极→导线→电源负极应用化学电源、金属的防护电镀、精炼铜、电冶金实例(电池反应)CuSO4+Zn===Cu+ZnSO42FeCl3+Cu===2FeCl2+CuCl2CuCl2=====Cu+Cl2↑2NaCl+2H2O=====2NaOH+Cl2↑+H2↑按如图所示装置进行实验,并回答下列问题:(1)判断装置的名称:A池为,B池为
(2)锌极为极,电极反应式为____________________________________________;铜极为极,电极反应式为_______________________________________________;石墨棒C1为极,电极反应式为___________________________________________;石墨棒C2附近发生的实验现象为
(3)当C2极析出224mL气体(标准状况)时,锌的质量(填“增加”或“减少”)g,CuSO4溶液的质量(填“增加”或“减少”)g
[审题指导]信息提取①A池中电极材料金属活动性不同,而B池中电极均为石墨棒;②A池中Zn棒与CuSO4溶液可发生氧化还原反应,而B池中石墨与KCl溶液不能反应