第三单元化学能与电能的转化第1课时化学能转化为电能化学电源【目标导航】1
通过实验探究认识化学能可以转化为电能及原电池的构成条件
知道干电池、充电电池、燃料电池等发展中的化学电源的特点
会书写简单的原电池的电极反应式及电池总反应方程式(离子方程式)
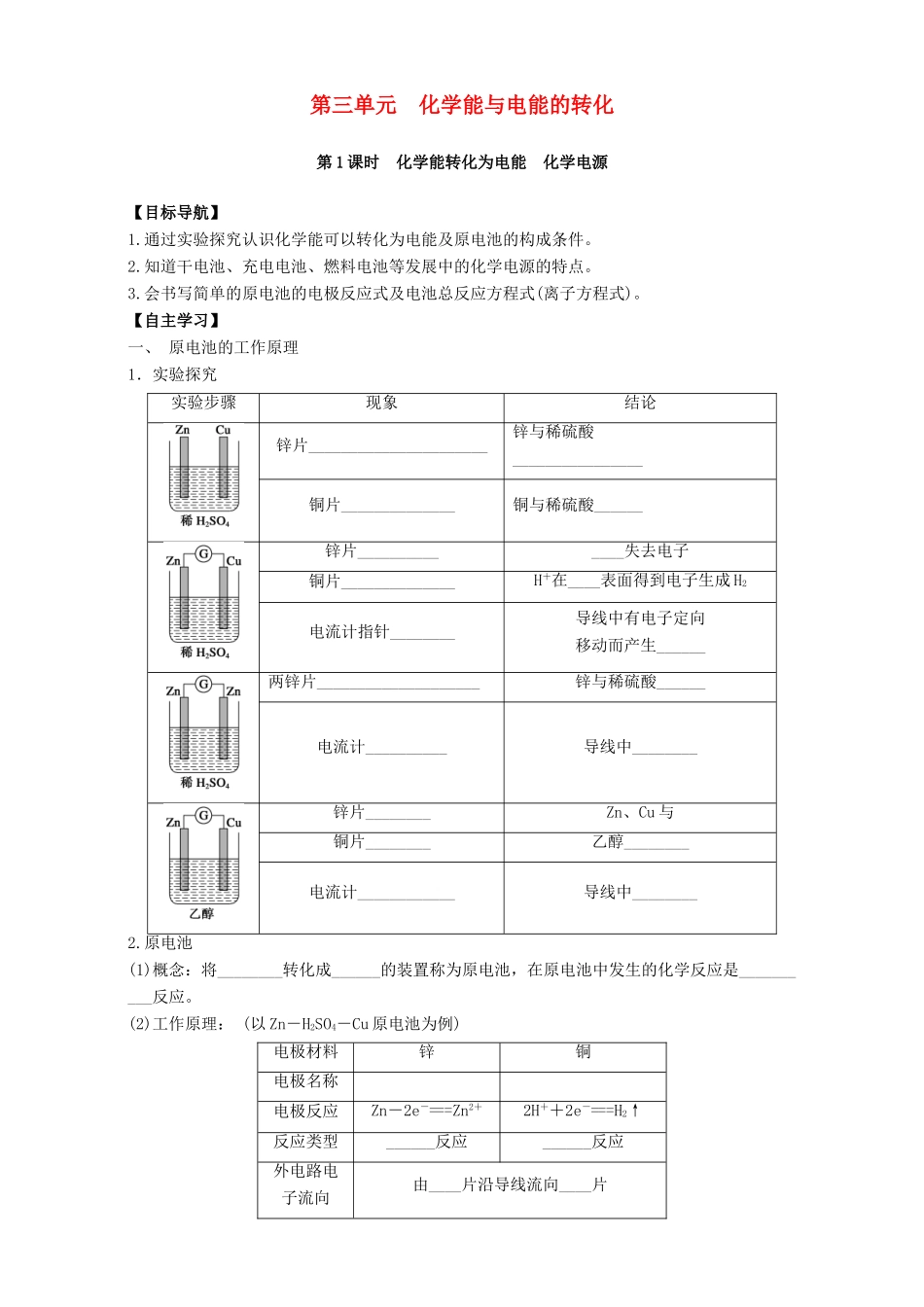
【自主学习】一、原电池的工作原理1.实验探究实验步骤现象结论锌片______________________锌与稀硫酸________________铜片______________铜与稀硫酸______锌片______________失去电子铜片______________H+在____表面得到电子生成H2电流计指针________导线中有电子定向移动而产生______两锌片____________________锌与稀硫酸______电流计__________导线中________锌片________Zn、Cu与铜片________乙醇________电流计____________导线中________2
原电池(1)概念:将________转化成______的装置称为原电池,在原电池中发生的化学反应是__________反应
(2)工作原理:(以Zn-H2SO4-Cu原电池为例)电极材料锌铜电极名称电极反应Zn-2e-===Zn2+2H++2e-===H2↑反应类型______反应______反应外电路电子流向由____片沿导线流向____片内电路离子移向溶液中____向正极移动,在____片上被还原为____原电池总反应Zn+2H+===Zn2++H2↑(3)构成条件:①本质→有自发进行的__________反应;②电极→有活泼性不同的两个电极(金属与金属或金属与能导电的非金属);③溶液→两电极插入________溶液或熔融电解质;④回路→形成闭合回路(电极插入电解质溶液,且两电极接触或用导线连接)
[议一议]1