第7讲化学反应速率与化学平衡[考纲要求]1
了解化学反应速率的概念和定量表示方法
能正确计算化学反应的转化率(α)
了解反应活化能的概念
了解催化剂的重大作用
了解化学反应的可逆性及化学平衡的建立
掌握化学平衡的特征
了解化学平衡常数(K)的含义,能利用化学平衡常数进行相关计算
理解外界条件(浓度、温度、压强、催化剂等)对反应速率和化学平衡的影响,能用相关理论解释其一般规律
了解化学反应速率和化学平衡的调控在生活生产和科学研究领域中的重要作用
[学科素养]1
变化观念与平衡思想:认识化学反应是有限度的,能多角度、动态地分析化学平衡状态并运用化学平衡移动原理解决实际问题
证据推理与模型认知:通过对化学平衡概念的深刻讨论,建立平衡思想,并能广泛应用于一定条件下的可逆过程中,揭示平衡移动的本质与规律
科学精神与社会责任:应具有严谨求实的科学态度,具有探索未知、崇尚真理的意识;赞赏化学对社会发展的重大贡献,具有可持续发展意识和绿色化学观念,能对与化学有关的社会热点问题做出正确的价值判断
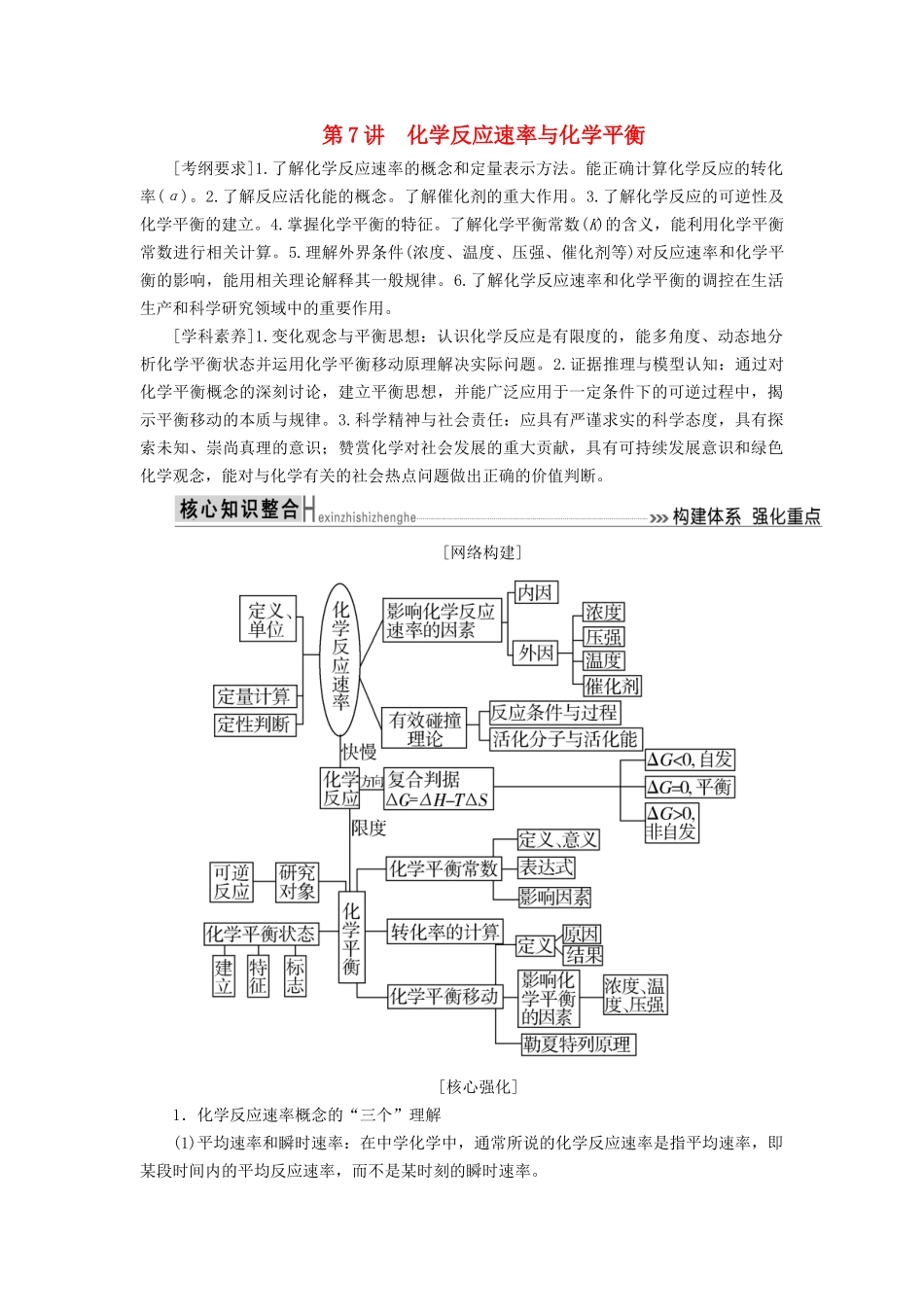
[网络构建][核心强化]1.化学反应速率概念的“三个”理解(1)平均速率和瞬时速率:在中学化学中,通常所说的化学反应速率是指平均速率,即某段时间内的平均反应速率,而不是某时刻的瞬时速率
(2)化学反应速率越快不等于化学反应现象越明显,如某些中和反应
(3)同一反应中,同一时间段内用不同物质的物质的量浓度变化表示的反应速率,数值可能不同,但意义相同,其数值之比等于化学方程式中对应物质的化学计量数之比
2.化学平衡状态判断的两个“标志”(1)v(正)=v(逆)
(2)各组分百分含量保持不变
以及能间接说明以上两点的其他“有条件标志”
3.用平衡移动原理判断平衡移动的方向如果改变影响平衡的一个条件(如浓度、压强或温度等),平衡就向着能够减弱这种改变的方向移动
(1)升高温度时,