第1课时二氧化硫的性质和作用[学习目标定位]1
会依据酸性氧化物的通性及硫元素的化合价分析理解二氧化硫的性质;知道二氧化硫具有漂白性
通过认识二氧化硫对空气的污染、酸雨的危害,增强环保意识
一、SO2的性质1.SO2的物理性质颜色状态气味密度溶解性毒性无气体刺激性比空气大易溶于水有毒2
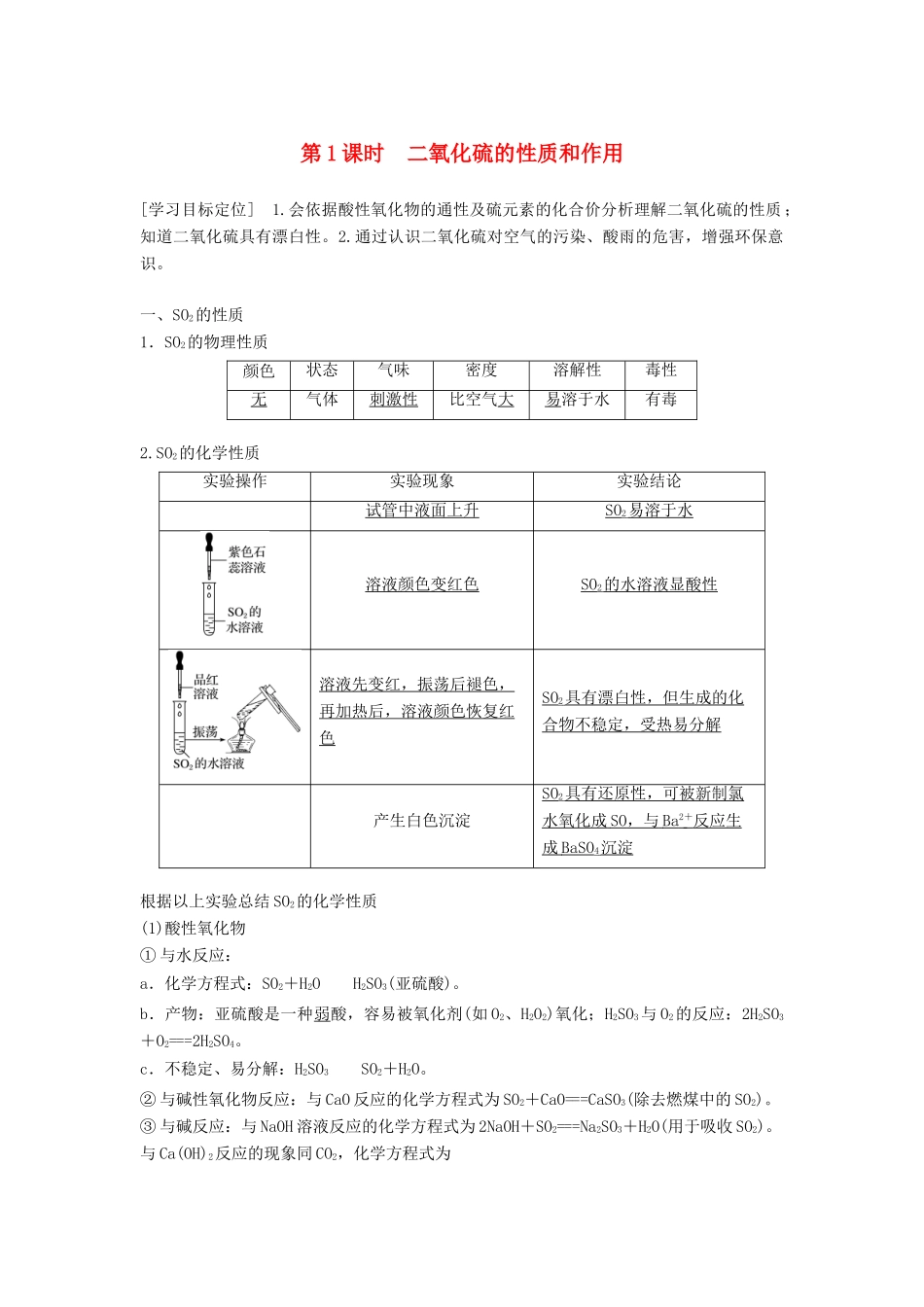
SO2的化学性质实验操作实验现象实验结论试管中液面上升SO2易溶于水溶液颜色变红色SO2的水溶液显酸性溶液先变红,振荡后褪色,再加热后,溶液颜色恢复红色SO2具有漂白性,但生成的化合物不稳定,受热易分解产生白色沉淀SO2具有还原性,可被新制氯水氧化成SO,与Ba2+反应生成BaSO4沉淀根据以上实验总结SO2的化学性质(1)酸性氧化物①与水反应:a.化学方程式:SO2+H2OH2SO3(亚硫酸)
b.产物:亚硫酸是一种弱酸,容易被氧化剂(如O2、H2O2)氧化;H2SO3与O2的反应:2H2SO3+O2===2H2SO4
c.不稳定、易分解:H2SO3SO2+H2O
②与碱性氧化物反应:与CaO反应的化学方程式为SO2+CaO===CaSO3(除去燃煤中的SO2)
③与碱反应:与NaOH溶液反应的化学方程式为2NaOH+SO2===Na2SO3+H2O(用于吸收SO2)
与Ca(OH)2反应的现象同CO2,化学方程式为Ca(OH)2+SO2===CaSO3↓+H2O、CaSO3+SO2+H2O===Ca(HSO3)2
(2)还原性SO2还原性较强,可被多种氧化剂[如O2、H2O2、X2(X=Cl、Br、I)、HNO3、KMnO4等]氧化
①与O2反应:2SO2+O2((((2SO3(可逆反应);②与H2O2反应:SO2+H2O2===H2SO4;③使酸性KMnO4溶液褪色;④使溴水褪色SO2+Br2+2H2O===H2SO4+2HBr
(3)弱氧化性SO2+2H2S===3S↓+