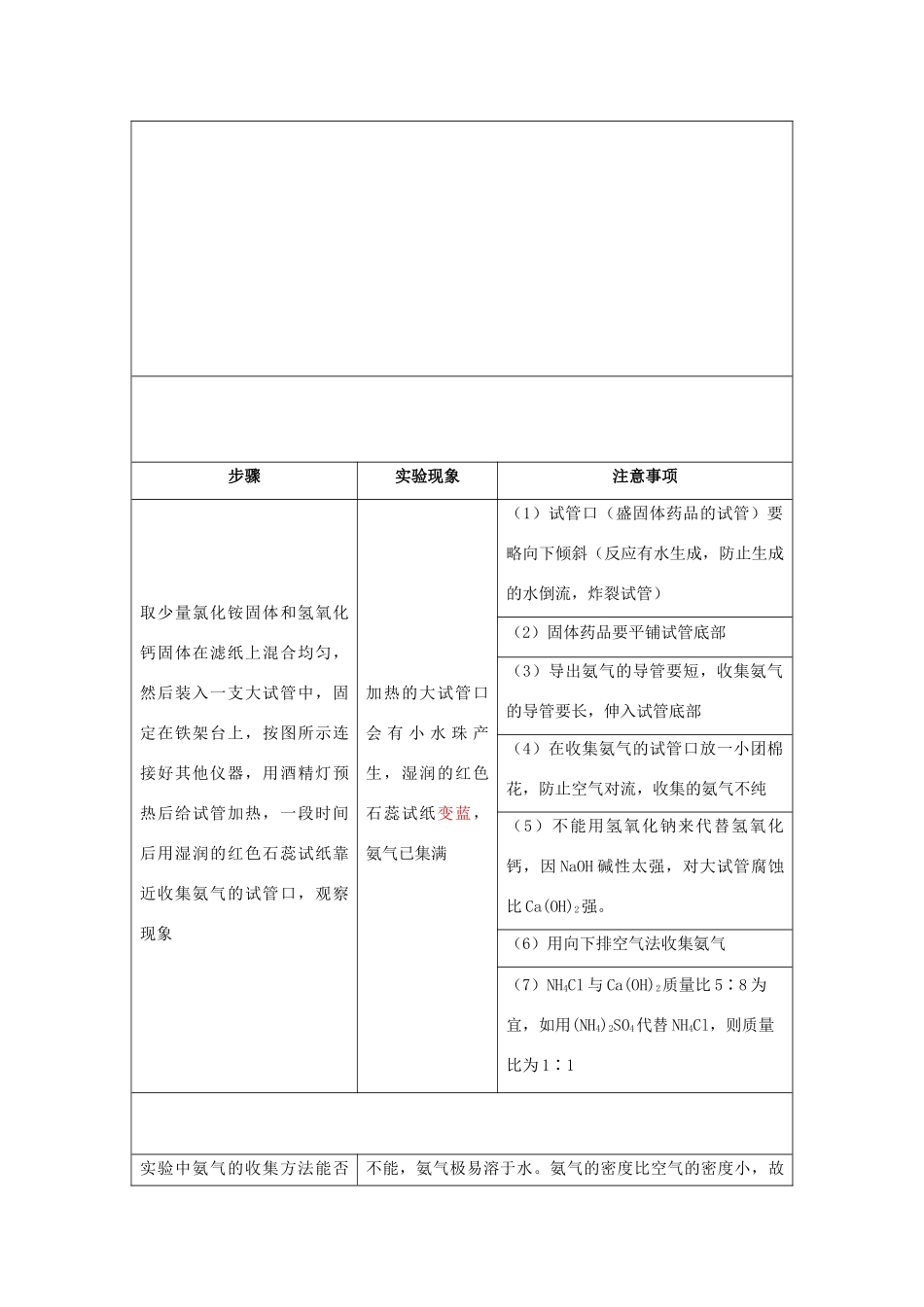
实验11氨的实验室制法氨的实验室制法1、制取氨气2、学会实验室制取氨气的原理和方法3、学会探究氨的多种制法方案(一)加热铵盐与碱的固体混合物2NH4Cl+Ca(OH)2===2NH3↑+2H2O+CaCl2(实验室一般制法)(二)加热浓氨水制氨气NH3·H2O===NH3↑+H2O(三)浓氨水中加入生石灰或碱NH3+H2ONH3·H2ONH+OH生石灰溶于水放出大量的热,加碱使得OH浓度增大,使平衡向左移动,产生大量的氨气大试管(2支)、酒精灯、铁架台(带铁圈)、单孔橡皮塞、导管、湿润的红色石蕊试纸、棉花、NH4Cl(s)、Ca(OH)2(s)步骤实验现象注意事项取少量氯化铵固体和氢氧化钙固体在滤纸上混合均匀,然后装入一支大试管中,固定在铁架台上,按图所示连接好其他仪器,用酒精灯预热后给试管加热,一段时间后用湿润的红色石蕊试纸靠近收集氨气的试管口,观察现象加热的大试管口会有小水珠产生,湿润的红色石蕊试纸变蓝,氨气已集满(1)试管口(盛固体药品的试管)要略向下倾斜(反应有水生成,防止生成的水倒流,炸裂试管)(2)固体药品要平铺试管底部(3)导出氨气的导管要短,收集氨气的导管要长,伸入试管底部(4)在收集氨气的试管口放一小团棉花,防止空气对流,收集的氨气不纯(5)不能用氢氧化钠来代替氢氧化钙,因NaOH碱性太强,对大试管腐蚀比Ca(OH)2强
(6)用向下排空气法收集氨气(7)NH4Cl与Ca(OH)2质量比5∶8为宜,如用(NH4)2SO4代替NH4Cl,则质量比为1∶1实验中氨气的收集方法能否不能,氨气极易溶于水
氨气的密度比空气的密度小,故用排水法
采用向下排空气法收集
要得到干燥的氨气我们应该怎么做
在两只试管中间连接一个盛有碱石灰的干燥管(氨气是碱性气体,且易和无水CaCl2形成CaCl2·8NH3,故用碱石灰做干燥剂)
检验氨气是否收集满的方法
a:将湿润的红色石蕊