第2课时电解原理的应用发展目标体系构建1
通过对电解饱和食盐水、电解精炼铜、电镀等电解实例的认知,认识电解在实现物质转化和储存能量中的重要作用
通过讨论电镀工业对环境造成的影响,提升“科学态度与社会责任”的学科素养
1.电解食盐水制备烧碱、氢气和氯气向上述实验中滴入酚酞溶液,接通电源后,哪个电极附近溶液的颜色发生了变化
提示:接通电源后,阴极区溶液变红色
原因:H2O电离出的H+放电,水的电离平衡右移,使c(OH-)增大,即阴极区产生碱,使酚酞变红色
2.铜的电解精炼(1)装置(2)粗铜成分①主要成分:Cu
②杂质金属:比铜活泼的有Zn、Fe、Ni等
比铜不活泼的有Ag、Pt、Au等
(3)电极反应微点拨:(1)粗铜中含Zn、Fe、Ag等杂质,同时间段内两电极改变的质量不相等,但两电极通过的电量相等
(2)电解过程中,阴离子浓度不变,Cu2+浓度减小,Fe2+、Zn2+、Ni2+浓度增大
3.电镀(1)定义:应用电解原理,在金属表面镀上一薄层金属或合金的方法
(2)目的:增强金属的抗腐蚀能力、耐磨性能或改善金属制品的外观
(3)根据电解原理,设计在铁钉上镀铜的实验方案电镀原理阳极:Cu-2e-===Cu2+阴极:Cu2++2e-===Cu电镀方案电极材料阳极:铜片阴极:铁钉电镀液CuSO4溶液镀件铁钉微点拨:电镀的特点:“一多、一少、一不变”
(1)一多:是指阴极上有镀层金属沉积;(2)一少:是指阳极上有镀层金属溶解;(3)一不变:是指电镀后,电解质溶液中的离子浓度保持不变
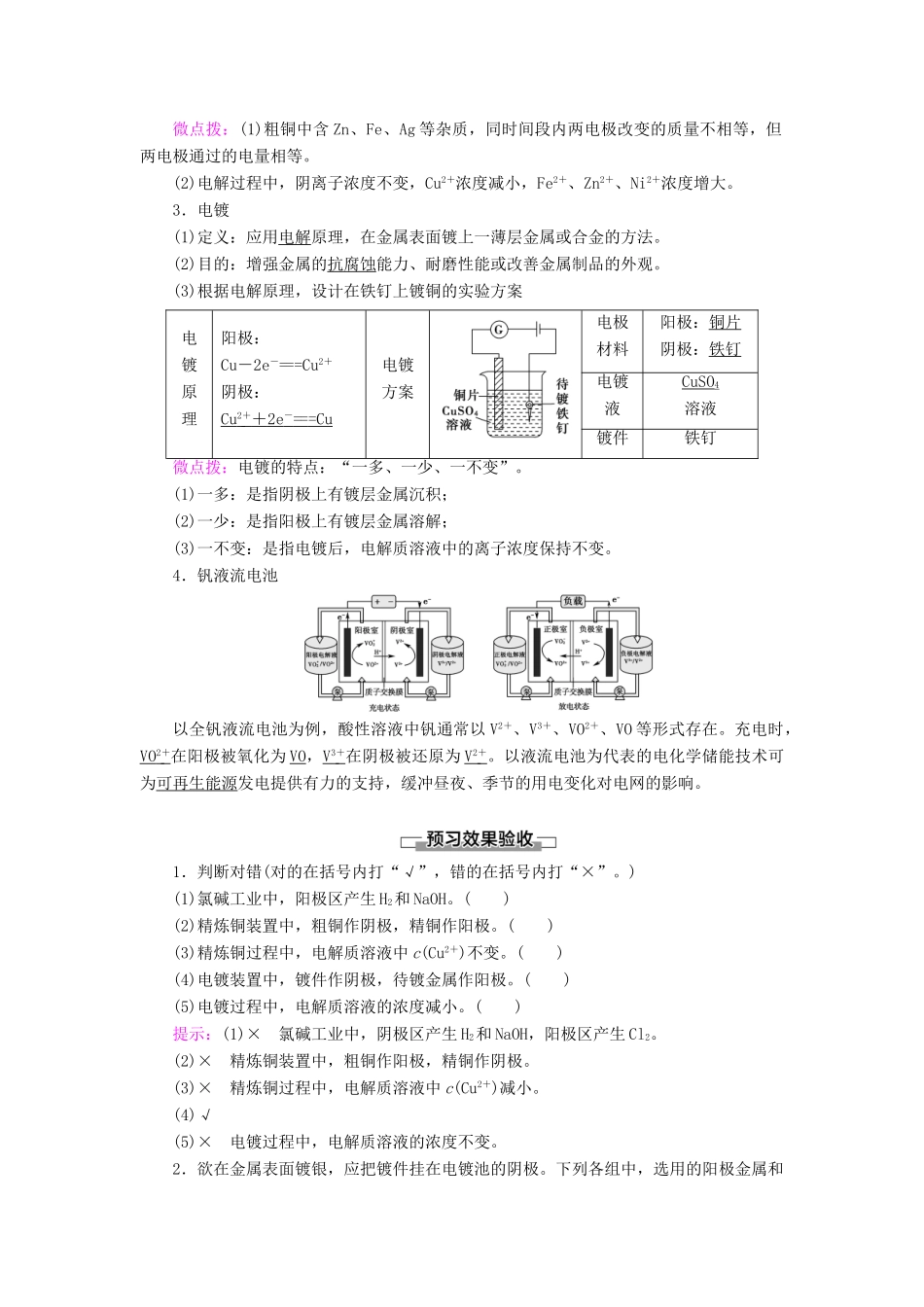
4.钒液流电池以全钒液流电池为例,酸性溶液中钒通常以V2+、V3+、VO2+、VO等形式存在
充电时,VO2+在阳极被氧化为VO,V3+在阴极被还原为V2+
以液流电池为代表的电化学储能技术可为可再生能源发电提供有力的支持,缓冲昼夜、季节的用电变化对电网的影响
1.判断对错(对的在括号内打“