第4讲物质结构与元素周期律[考纲要求]1
了解元素、核素和同位素的含义
了解原子的构成;了解原子序数、核电荷数、质子数、中子数、核外电子数以及它们之间的相互关系
了解原子核外电子排布规律
掌握元素周期律的实质;了解元素周期表(长式)的结构(周期、族)及其应用
以第3周期为例,掌握同一周期内元素性质的递变规律与原子结构的关系
以ⅠA和ⅦA族为例,掌握同一主族内元素性质的递变规律与原子结构的关系
了解金属、非金属在周期表中的位置及其性质递变规律
了解化学键的定义;了解离子键、共价键的形成
了解物质的组成、结构和性质的关系
[学科素养]1
变化观念:认识元素性质呈现周期性变化的根本原因是元素原子的核外电子排布呈现周期性变化,元素周期表是元素周期律的表现形式,能利用元素的位置、原子的结构等与元素性质的关系解决实际问题
模型认知:能运用原子结构示意图、电子层模型解释核外电子排布的周期性变化,揭示元素性质周期性变化的本质
科学探究:能够发现和提出有探究价值的元素性质递变规律问题,确定探究目的,设计探究方案,进行实验探究,能根据实验现象总结规律,并勇于提出自己的独到见解
社会责任:能利用元素周期律对生产、生活进行指导,有效解决生产、生活中的实际问题
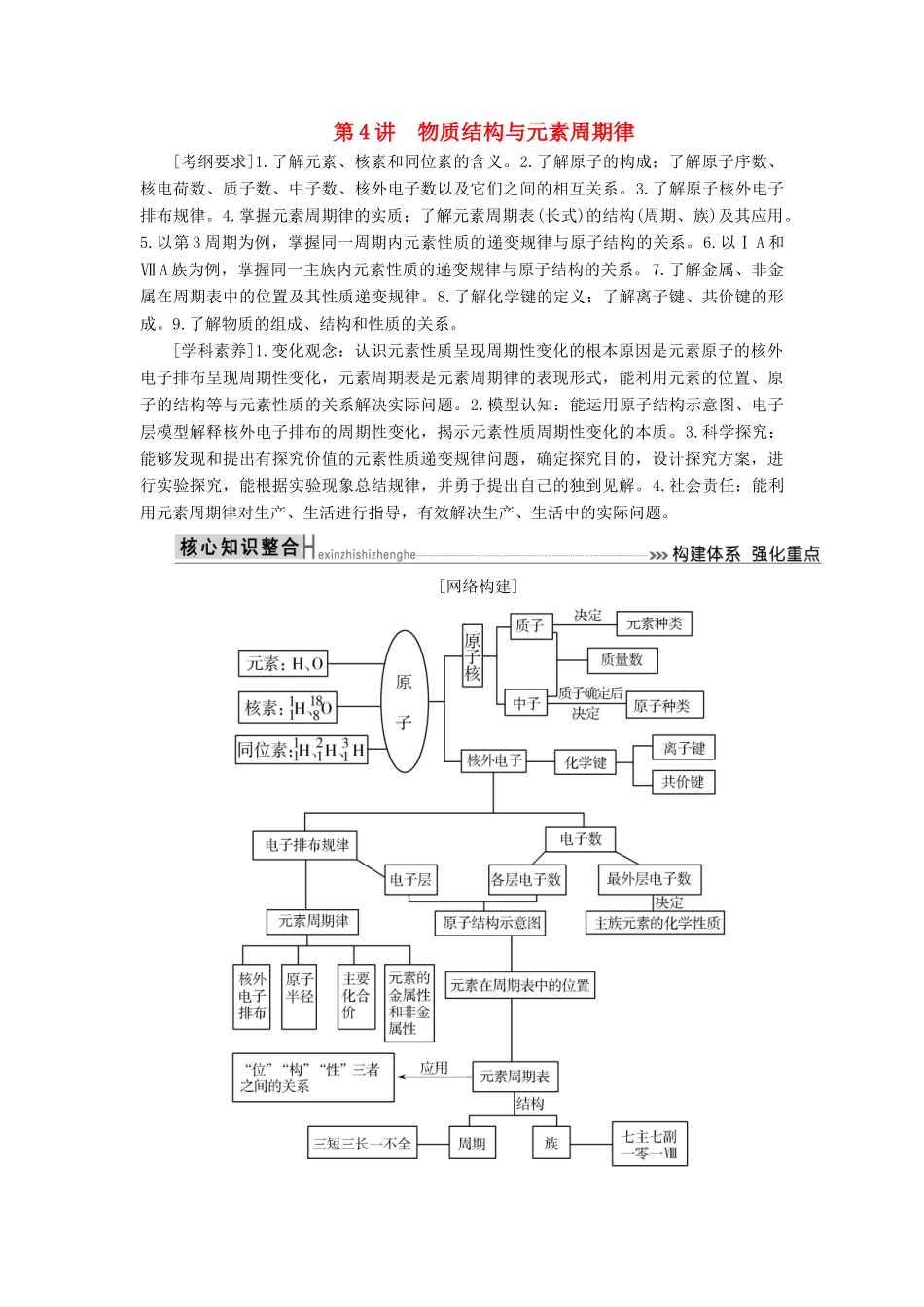
[网络构建][核心强化]1.必考的一个微粒(X)和四个“关系式”(1)质子数=核电荷数=核外电子数=原子序数
(2)质量数=质子数+中子数
(3)质子数=阳离子的核外电子数+阳离子所带电荷数
(4)质子数=阴离子的核外电子数-阴离子所带电荷数
2.元素周期律中必考的两类“比较”(1)元素金属性、非金属性强弱的比较
(2)微粒半径大小的比较依据:周期表中位置和微粒电子层结构
3.常考的两个主族、一个周期(1)碱金属和卤族元素性质递变规律
(2)第三周期元素性质递变规律
4.短周期中常考的元素:H、C、