钠及其化合物〖复习目标〗1.了解钠及其重要化合物的主要性质和重要应用
2.运用元素周期律理解IA族元素(单质、化合物)的相似性和递变性
3.了解Na+、K+等常见离子的检验方法
〖知识清单〗考点一钠及其氧化物一、钠的性质与应用1.钠的原子结构及存在2.钠的物理性质3.钠的化学性质⑴钠与氧气反应⑵钠与氯气反应⑶与H2O反应⑷与熔融金属卤化物的反应4.钠的制备与用途⑴钠的制备⑵钠的用途①钠钾合金用于核反应的热交换剂;②制高压钠灯;③冶炼较特殊的金属,如钛、锆、铌、钽
二、氧化钠与过氧化钠化学式Na2ONa2O2阳、阴离子数比Na+与O2-之比为Na+与O22-之比为氧的化合价类别(不属于碱性氧化物)与H2O反应与CO2反应与盐酸反应稳定性不稳定较稳定用途〖典型例析〗例1.在一定条件下,将钠与氧气反应的生成物1
5g溶于水,所得溶液恰好能被80mL浓度为0
50mol/L的HCl溶液中和,则该生成物的成分是()A.Na2OB.Na2O2C.Na2O和Na2O2D.Na2O2和NaO2例2.将3
72g由钠、氧化钠和过氧化钠组成的混合物与足量水反应,在标准状况下生成672mL混合气体
将该混合气体用电火花点燃,恰好完全反应,则原混合物中钠、氧化钠、过氧化钠的物质的量之比为()A
3∶2∶1B
4∶2∶1C
1∶1∶1D
2∶1∶1例3.过氧化钠可作为氧气的来源
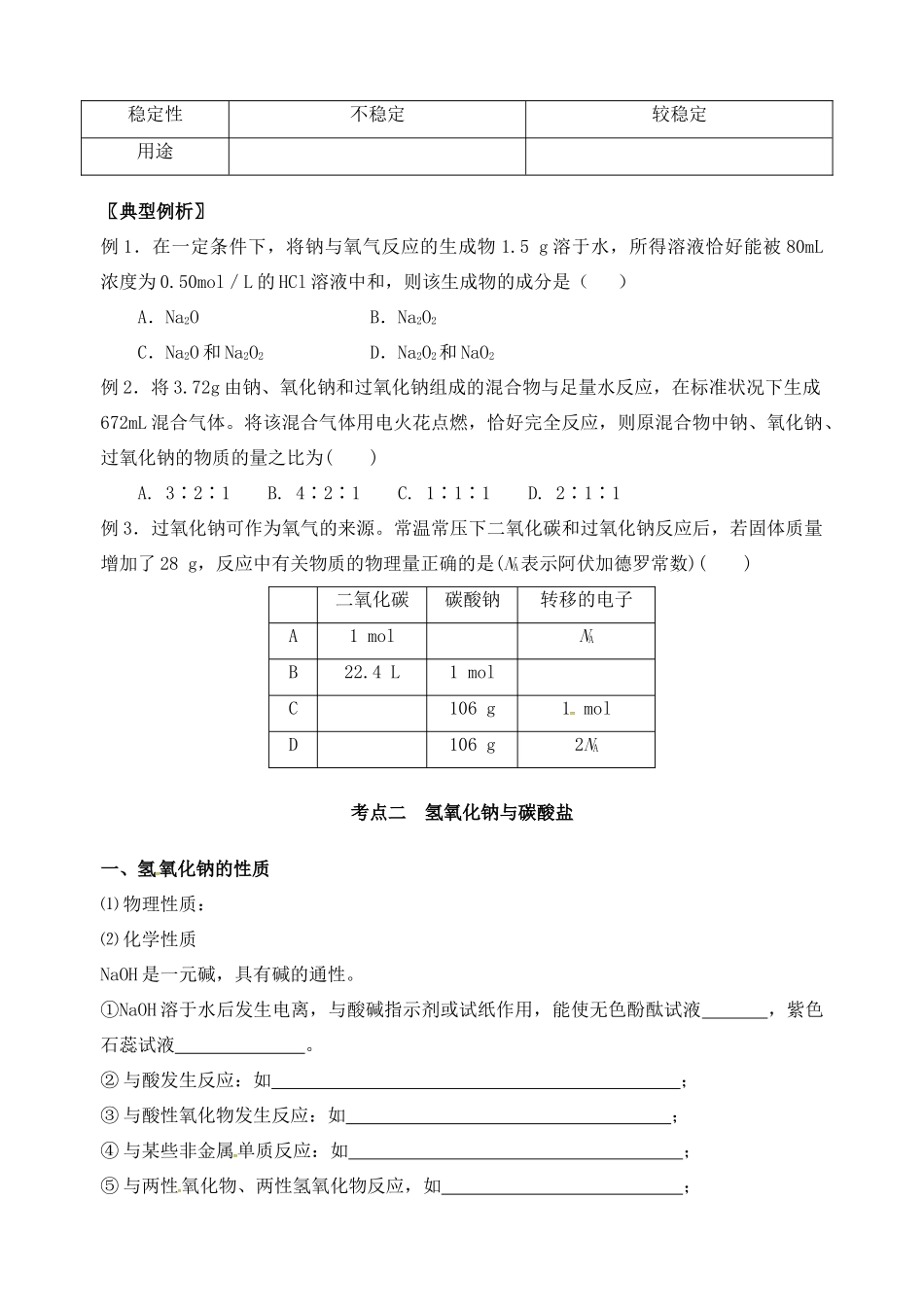
常温常压下二氧化碳和过氧化钠反应后,若固体质量增加了28g,反应中有关物质的物理量正确的是(NA表示阿伏加德罗常数)()二氧化碳碳酸钠转移的电子A1molNAB22
4L1molC106g1molD106g2NA考点二氢氧化钠与碳酸盐一、氢氧化钠的性质⑴物理性质:⑵化学性质NaOH是一元碱,具有碱的通性
①NaOH溶于水后发生电离,与酸碱指示剂或试纸作用,能使无色酚酞试液,紫色石蕊试液
②与酸发生反应:如;③与酸性氧化物发生