硫、氮和可持续发展本专题在高考命题中出现概率较大的考点是1.考查S、SO2、H2SO3、H2SO4等物质的性质及应用
2.考查N2、NO、NO2、NH3、NH3·H2O、HNO3等物质的性质及应用
3.考查NH3、HNO3、H2SO4的工业制法
4.考查SO2、NH3的实验室制法
5.考查SO2、NH3等气体及SO、NH等离子的检验方法
6.考查SO2、NO、NO2等物质对环境的影响
7.考查有关含硫、含氮物质的化学计算和实验
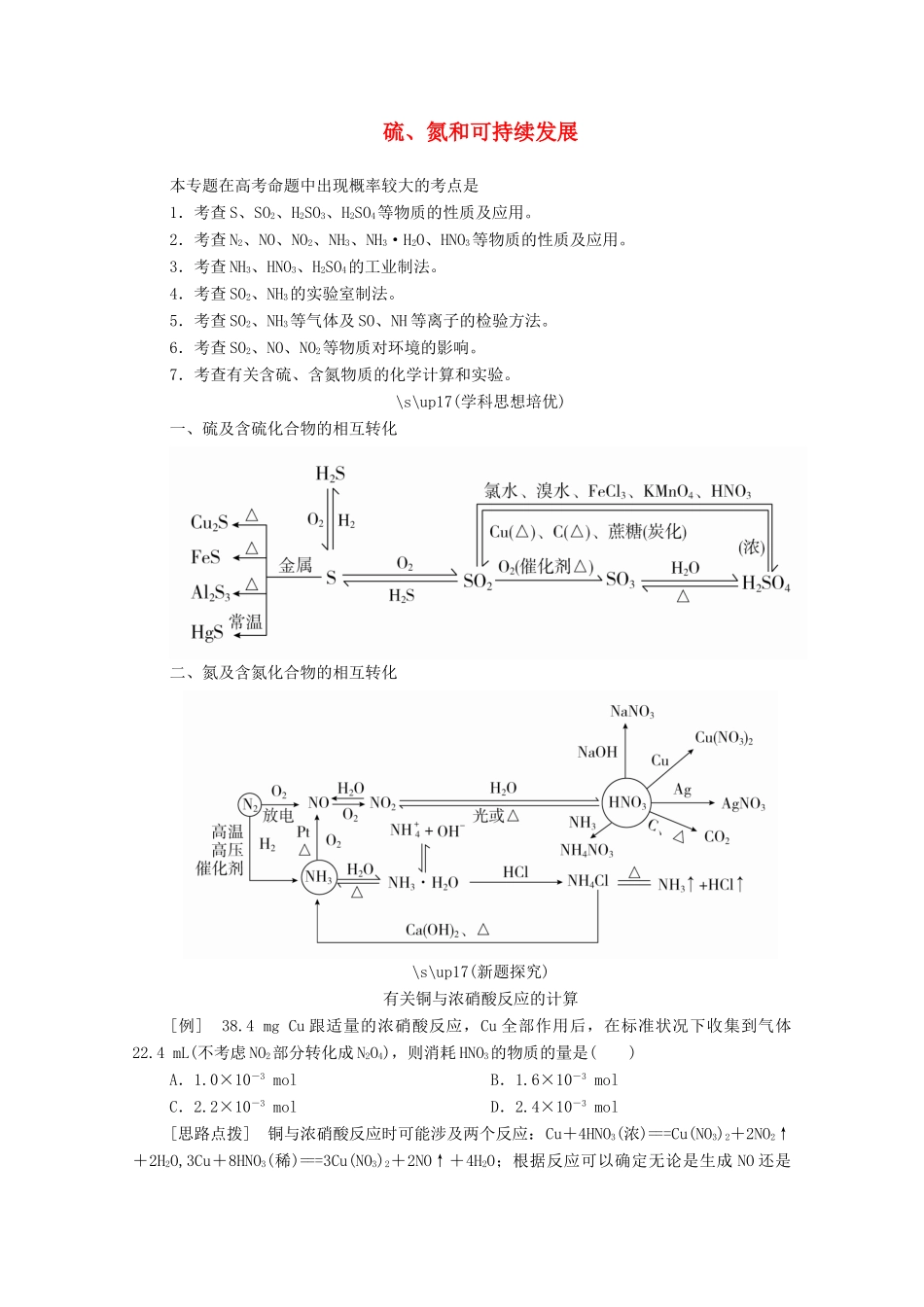
\s\up17(学科思想培优)一、硫及含硫化合物的相互转化二、氮及含氮化合物的相互转化\s\up17(新题探究)有关铜与浓硝酸反应的计算[例]38
4mgCu跟适量的浓硝酸反应,Cu全部作用后,在标准状况下收集到气体22
4mL(不考虑NO2部分转化成N2O4),则消耗HNO3的物质的量是()A.1
0×10-3molB.1
6×10-3molC.2
2×10-3molD.2
4×10-3mol[思路点拨]铜与浓硝酸反应时可能涉及两个反应:Cu+4HNO3(浓)===Cu(NO3)2+2NO2↑+2H2O,3Cu+8HNO3(稀)===3Cu(NO3)2+2NO↑+4H2O;根据反应可以确定无论是生成NO还是NO2或既生成NO又生成NO2,1mol气体均对应1molHNO3被还原,而1molCu→1molCu(NO3)2对应2molHNO3未被还原
故反应的HNO3可以分成两部分来求算
[解析]解法一:极限法
(1)从极限的观点分析,38
4mgCu若与浓硝酸完全反应生成标准状况下26
88mLNO2;若与稀硝酸反应放出标准状况下8
96mLNO,而实际收集到22
4mL气体,说明Cu和适量浓硝酸反应过程中开始浓度较大,后来浓度逐渐减小,所以收集到的气体为NO2和NO的混合气体
(2)按平行计算,设和稀硝酸反应的Cu的物质的量为3x,和浓硝酸反应的C