第二课时元素周期表和元素周期律的应用学习目标:1
知道元素周期表的简单分区,进一步认识元素周期表是元素周期律的具体表现形式
学会运用元素周期表、元素周期律的有关知识,指导科学研究和工农业生产
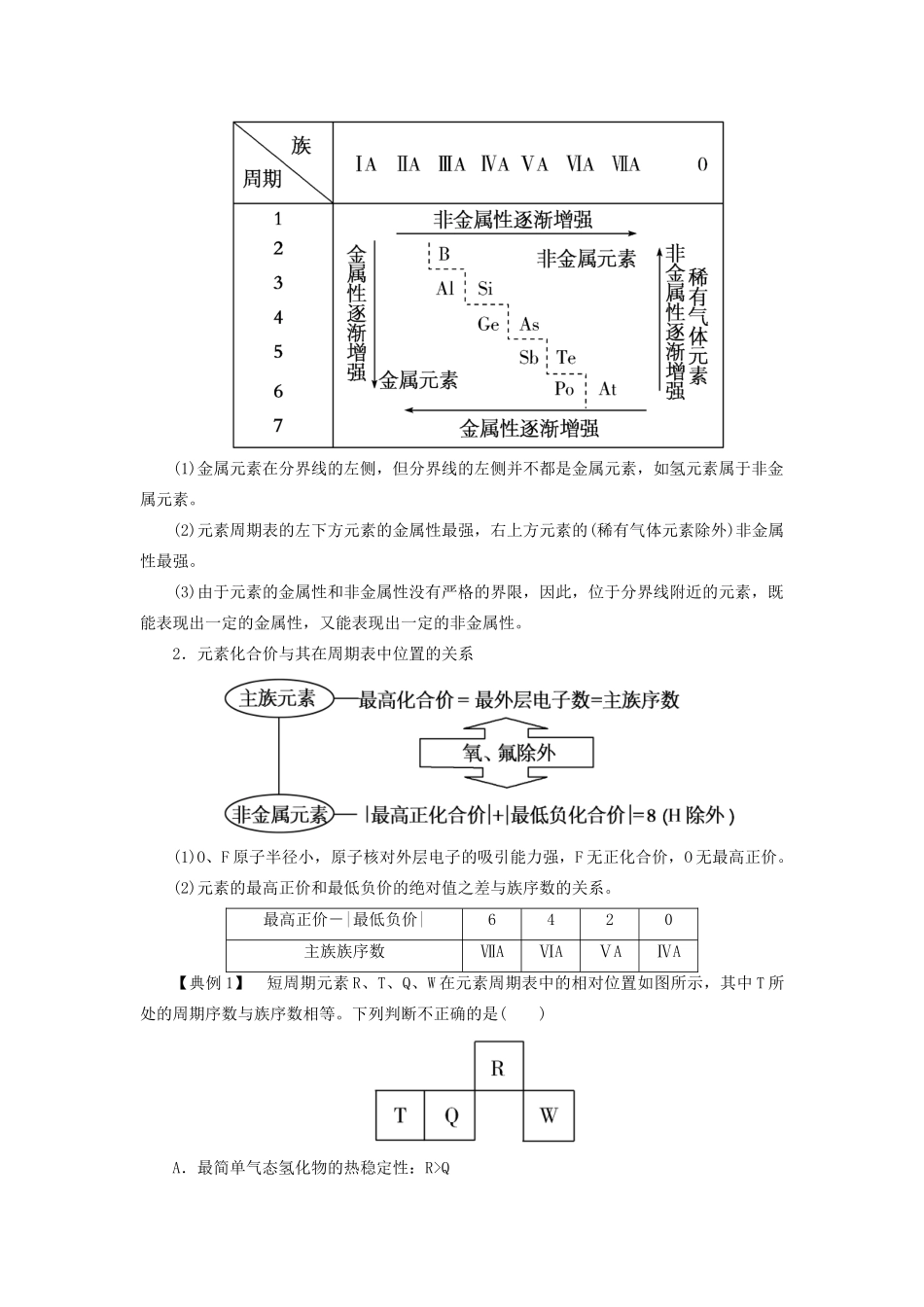
1.金属元素与非金属元素的分区及性质递变规律(1)分界线的划分:沿着周期表中B、Si、As、Te、At跟Al、Ge、Sb、Po之间画一条虚线,虚线的左下方是金属元素,右上方是非金属元素
(2)元素的金属性和非金属性之间没有严格的界线
分界线附近的元素,既能表现出一定的金属性,又能表现出一定的非金属性
(3)周期表的左下方金属性最强的元素是铯元素(放射性元素除外);右上方非金属性最强的元素是氟元素;最后一个纵行是0族元素
2.元素的化合价与元素在周期表中的位置之间的关系主族元素的最高正化合价等于原子所能失去或偏移的最外层电子数,而非金属的负化合价则等于使原子达到8电子稳定结构所需得到的电子数
所以,非金属元素的最高正化合价和它的负化合价的绝对值之和等于8
(1)周期序数=电子层数
(2)最高正价=最外层电子数=主族序数=8-|最低负价|(其中,F无正价,O无最高正价)
(3)最低负价=主族序数-8
3.元素周期表和元素周期律的应用(1)根据同周期、同主族元素性质的递变规律判断元素性质的强弱(或大小)
(2)应用于元素“位置—结构—性质”的相互推断
(3)预测新元素为新元素的发现及预测它们的原子结构和性质提供线索
(4)寻找新物质①在金属与非金属分界线附近寻找半导体材料
②研究氟、氯、硫、磷附近元素,制造新农药
③在过渡元素中寻找催化剂和耐高温、耐腐蚀的合金材料
1.判断正误(正确的打“√”,错误的打“×”)(1)最外层电子数相同的元素性质一定相似()(2)第三周期元素的最高正价等于它所处的主族序数()(3)原子及离子的核外电子层数等于该元素所在的周期数()(4)原子最外层电子数大于3