高考总复习·化学第一节化学反应的热效应灵山县武利中学邓海明高考总复习·化学1
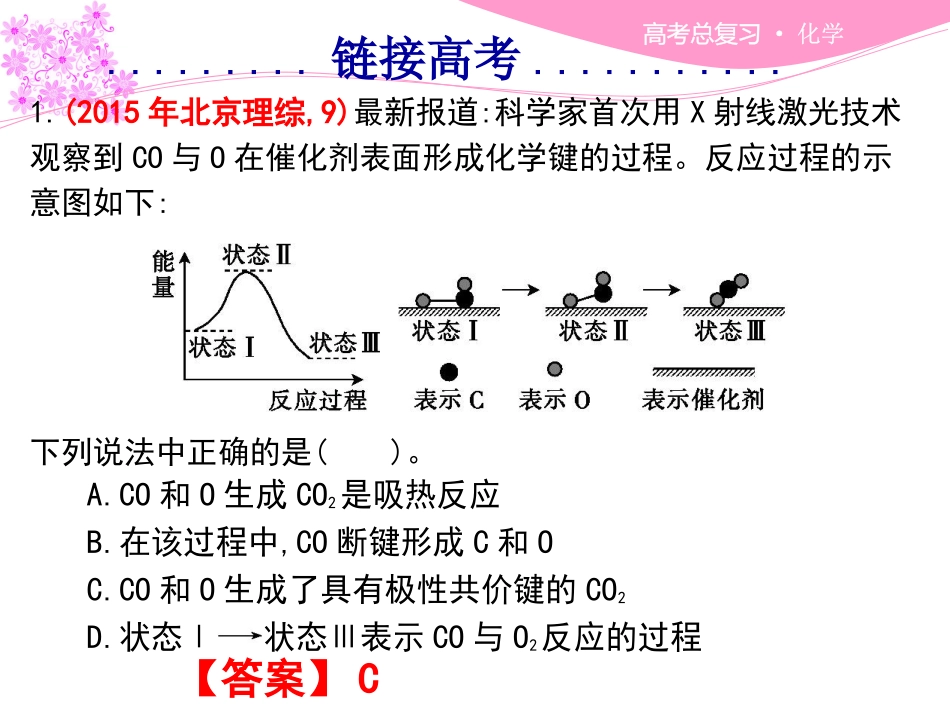
(2015年北京理综,9)最新报道:科学家首次用X射线激光技术观察到CO与O在催化剂表面形成化学键的过程
反应过程的示意图如下:下列说法中正确的是()
CO和O生成CO2是吸热反应B
在该过程中,CO断键形成C和OC
CO和O生成了具有极性共价键的CO2D
状态Ⅰ状态Ⅲ表示CO与O2反应的过程【答案】C
高考总复习·化学教材选修4讲到“化学反应过程中能量变化图像与吸热反应、放热反应的关系”;教材必修2讲到“极性键和非极性键的定义”
高考总复习·化学1、了解化学能与热能的相互转化,了解吸热反应、放热反应和反应热等概念
2、了解热化学方程式的含义,能正确书写热化学方程式
3、了解盖斯定律,能计算化学反应焓变
考纲目标:高考总复习·化学1
焓变、反应热的概念(1)反应热:化学反应过程中的能量
(2)焓变:条件下的反应热,称之为焓变,符号为,单位为
一、焓变、反应热ΔHkJ·mol-1kJ/mol恒压吸收或释放放热反应:吸热反应:ΔH<0或ΔH为“-”ΔH>0或ΔH为“+”高考总复习·化学2
吸热反应和放热反应(1)从反应物和生成物的总能量相对大小的角度分析(如图所示)放热反应:反应物的总能量生成物的总能量吸热反应:反应物的总能量生成物的总能量吸热反应放热反应放热反应吸热反应填“>”“