化学Ⅱ第一节元素周期表第一章物质结构元素周期律第三课时卤族元素[思考与交流]推测氟、氯、溴、碘原子结构的共同点和不同点
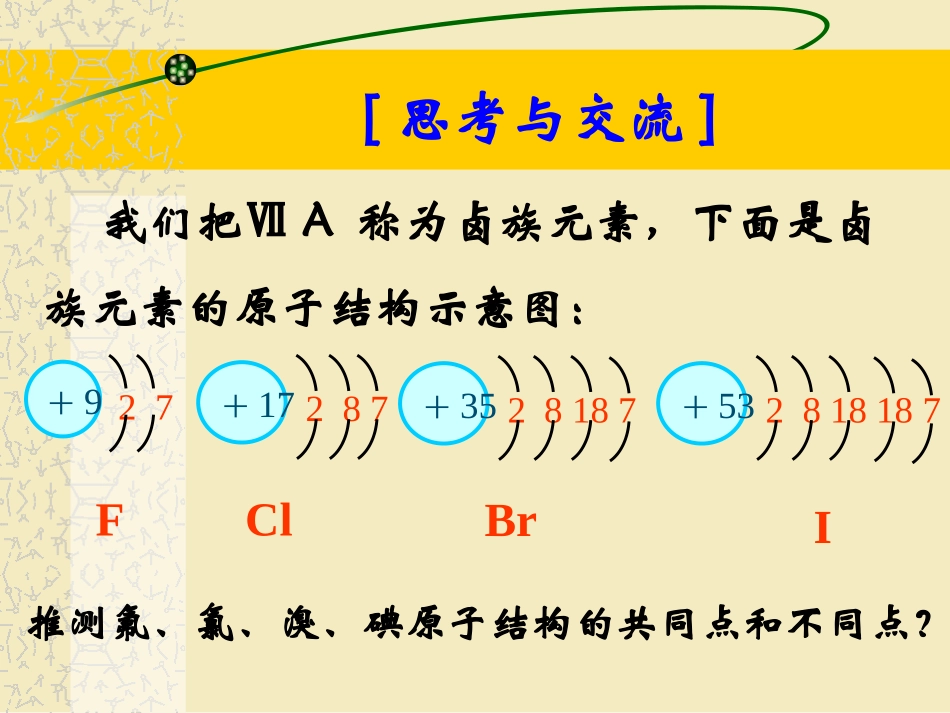
我们把ⅦA称为卤族元素,下面是卤族元素的原子结构示意图:+927+17287+3528187+532818187FClBrI最外层电子数均为,均易电子,具有强性
一、卤素原子结构特点随着核电荷数的递增,电子层数逐渐,原子半径逐渐
(1)相似性:(2)递变性:7得到氧化增多增大二、卤素单质的物理性质(1)相似性:(2)递变性:有颜色,密度小,熔沸点都较低
阅读教材P8:资料卡片颜色:状态:密度:熔沸点:逐渐加深气→液→固逐渐增大依次增高三、卤素单质与H2的反应名称反应条件方程式氢化物稳定性F2Cl2Br2I2冷暗处爆炸H2+F2=2HFHF很稳定光照或点燃H2+Cl2=2HClHCl稳定加热H2+Br2=2HBrHBr较不稳定不断加热,缓慢进行H2+I2=2HIHI很不稳定三、卤素单质与H2的反应F2Cl2Br2I2反应越来越难HF>HCl>HBr>HI与H2剧烈程度:生成的氢化物的稳定性:水溶液酸性:HF<HCl<HBr<HI四、卤素单质之间的置换反应实验操作实验现象化学方程式将少量氯水加入NaBr溶液中,用力振荡后加少量CCl4,振荡,静置静置后,液体分层,上层,下层
将少量氯水加入KI溶液中,用力振荡后加少量CCl4,振荡,静置静置后,液体分层,上层,下层
将少量溴水加入KI溶液中,用力振荡后加少量CCl4,振荡,静置静置后,液体分层,上层,下层
无色橙红色无色紫红色无色紫红色2NaBr+Cl2=2NaCl+Br22KI+Cl2=2KCl+I22KI+Br2=2KBr+I2由上述反应可比较卤素单质____性强弱
氧化氧化性:F2>Cl2>Br2>I2★从F→I,元素的非金属性逐渐减弱
相应卤素离子的还原性由强到弱的顺序是:I->Br->Cl->F-四、