镁铝一、镁、铝及其化合物(一)金属镁、铝性质的比较1、周期表中的位置及化合价:2、物理性质的比较:3、化学性质的比较:共同点:性,能与反应
不同点及其结构原因:镁的化学性质铝的化学性质与氧气、氯气反应与氮气、氯气、硫等反应与H2O反应与氧化物反应与H+反应与氧化性酸反应与盐溶液反应与强碱溶液反应4、用途:注意:铝热反应实验药品:实验装置:实验现象:化学方程式:Fe2O3+Al(用途:)MnO2+Al(二)镁及镁的化合物之间的转化(三)、铝的化合物1、氧化铝:氧化物(1)与H+反应(2)与强碱(OH-)反应2、氢氧化铝:氢氧化物,不稳定:氢氧化铝的电离方程式:(1):与H+反应(2)与强碱(OH-)反应小结:Al3+、Al(OH)3、AlO2-的相互转化Al(OH)3AlAlO2(3)制取3、氯化铝与强碱(OH-)反应及其图象:4、偏铝酸钠与强酸(H+-)反应及其图象:5、硫酸铝钾(1)电离方程式:(2)与强碱(NaOH)反应强碱(NaOH)量少:强碱(NaOH)量多:(3)与强碱Ba(OH)2反应强碱Ba(OH)2量少:强碱Ba(OH)2量多:(4)明矾用途:
(三)铝及铝的化合物之间的转化二、典型例题:例1在硝酸铝和硝酸镁的混合溶液中,逐滴加入稀氢氧化钠溶液,直至过量
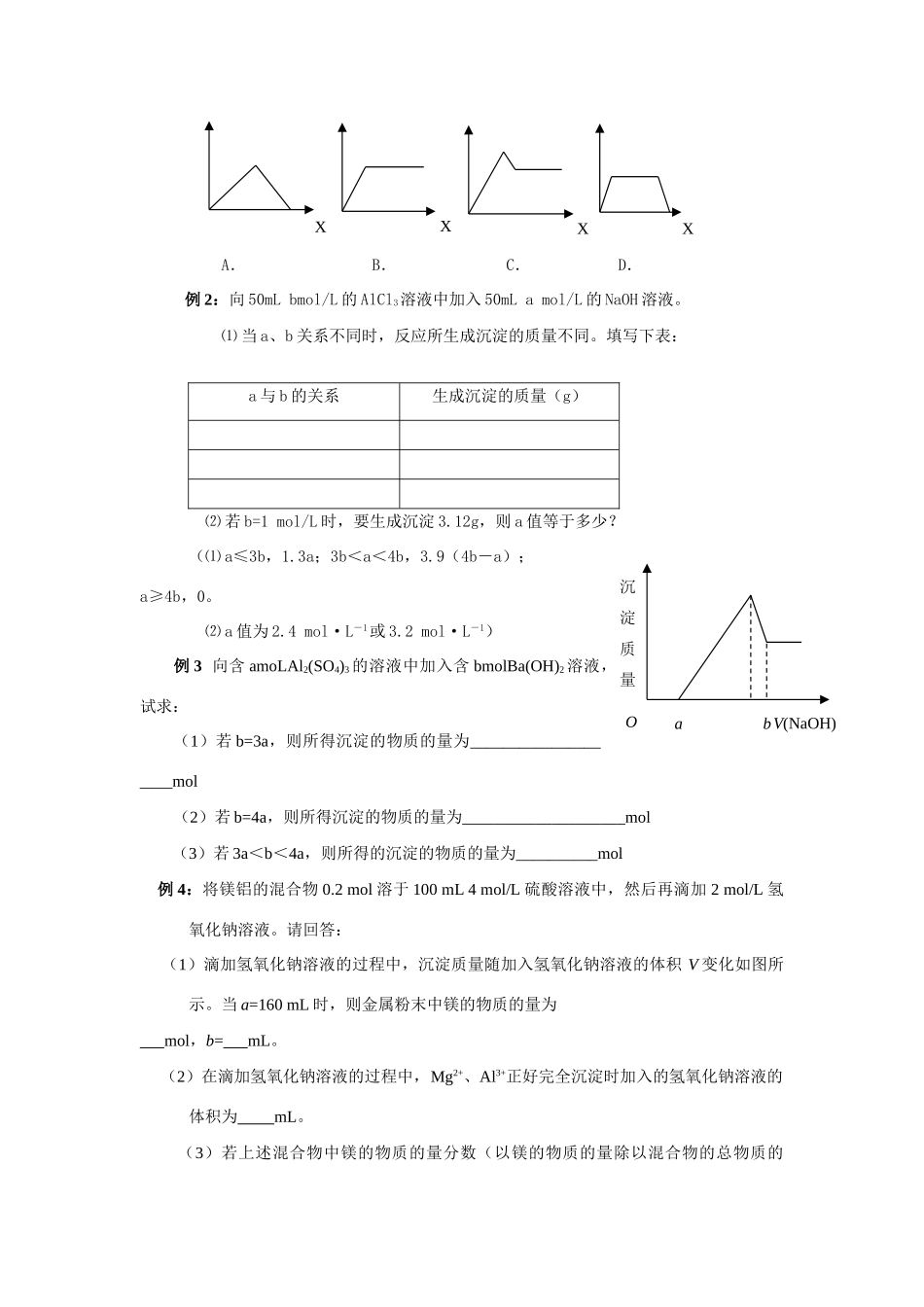
下列表示氢氧化钠加入量(X)与溶液中沉淀物的量(Y)的关系示意图中正确的是(C)A.B.C.D.例2:向50mLbmol/L的AlCl3溶液中加入50mLamol/L的NaOH溶液
⑴当a、b关系不同时,反应所生成沉淀的质量不同
填写下表:a与b的关系生成沉淀的质量(g)⑵若b=1mol/L时,要生成沉淀3
12g,则a值等于多少
(⑴a≤3b,1
3a;3b<a<4b,3
9(4b-a);a≥4b,0
4mol·L-1或3
2mol·L-1)例3向含amoLAl2(SO4)3的溶液中加入含bm