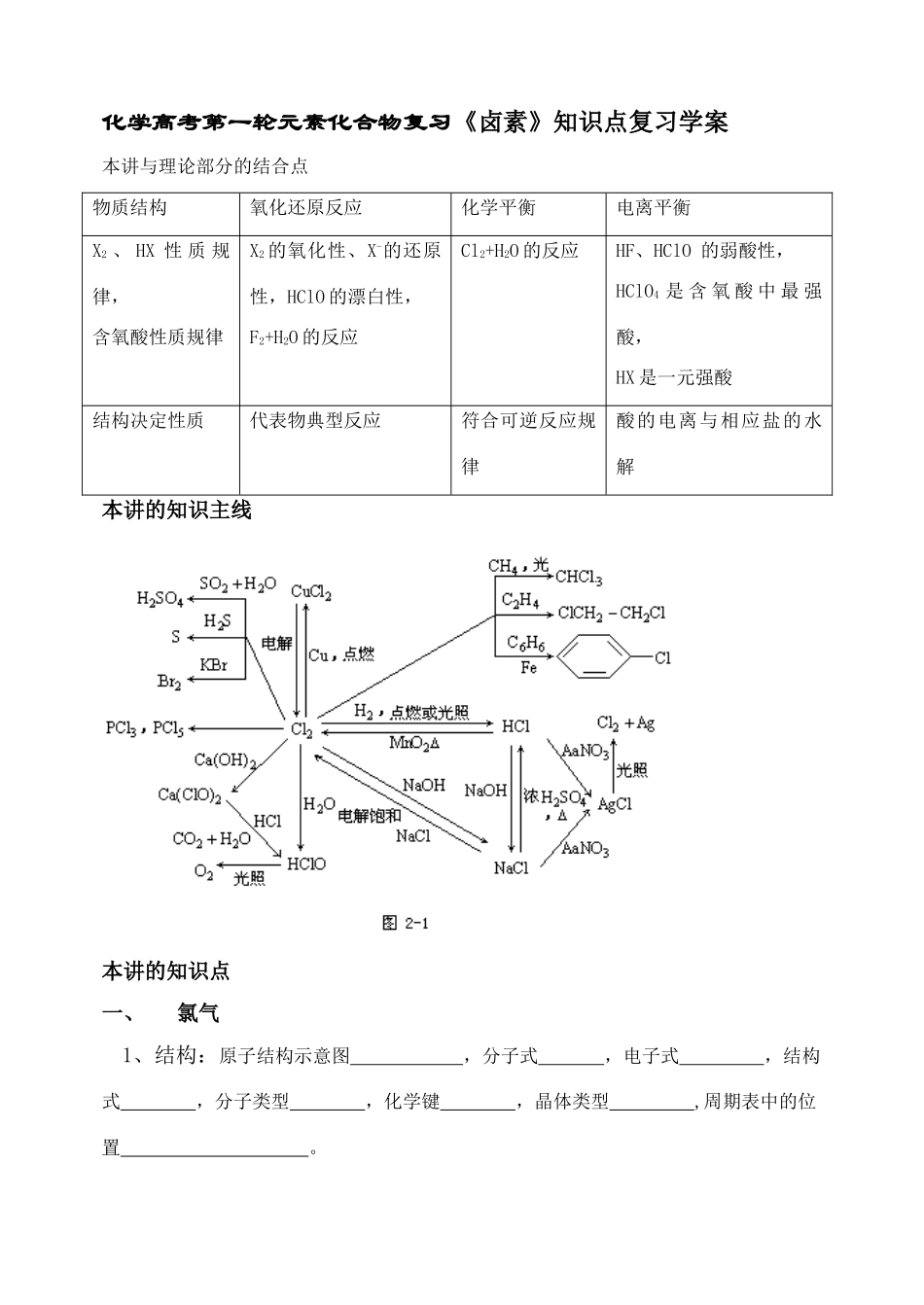
化学高考第一轮元素化合物复习《卤素》知识点复习学案本讲与理论部分的结合点物质结构氧化还原反应化学平衡电离平衡X2、HX性质规律,含氧酸性质规律X2的氧化性、X-的还原性,HClO的漂白性,F2+H2O的反应Cl2+H2O的反应HF、HClO的弱酸性,HClO4是含氧酸中最强酸,HX是一元强酸结构决定性质代表物典型反应符合可逆反应规律酸的电离与相应盐的水解本讲的知识主线本讲的知识点一、氯气1、结构:原子结构示意图,分子式,电子式,结构式,分子类型,化学键,晶体类型,周期表中的位置
2、物理性质:通常色,味的,比空气,毒,溶于水,液化,闻有毒气体的方法是
3、化学性质:(1)与非金属①与氢气:现象②与磷:现象(2)与金属①与钠:,现象
②与铜:现象,加水后现象③与铁:现象,但干燥氯气不与铁反应,故可用储运氯气
注意:①烟、雾气的区别:②燃烧的定义:(3)与水:,离子方程式①氯气溶于水叫氯水,氯水呈色
氯水成分:新制,久置,原因
新制氯水具有哪些性质
②HClO具有哪些性质
③HCl具有哪些性质
(4)与碱:①与NaOH:,离子方程式②与Ca(OH)2:,离子方程式③漂白粉制法,成分,保存,变质原因,发挥漂白性的原因
(5)氯气与还原性物质反应:①与NaBr:②与KI:③与Na2S:④与H2S:离子方程式⑤与FeCl2:⑥与FeBr2:(少,过量)⑦与FeI2:(少,过量)⑧与SO2混合通入水中:⑨与Na2SO3:(6)氯气与有机物反应:①与CH4:现象②与乙烯:③与乙炔:4、存在:5、用途:消毒,制盐酸,漂白粉,农药,氯仿等
6、制法:(1)工业制法:(2)实验室制法:原理:①发生:②净化:③收集方法:④尾气处理:⑤验满:二、卤族元素1、卤素原子结构的相似性和递变性相似性:最外层电子数均为________个.递变性:电子层数逐渐________.2、卤族元素性质的相似