山东省临朐县实验中学高一化学必修一学案:化学中常用的物理量—物质的量(第三课时)知识目标1、掌握一种新的表示溶液组成的方法——物质的量浓度,了解引入物质的量浓度的意义
2、掌握溶液体积、物质的量浓度和溶质的物质的量三者之间的关系
3、掌握配制一定物质的量浓度的溶液的实验方法,并且可以初步进行实验误差分析
学点一物质的量浓度1、概念:溶液里所含溶质B的
2、符号及单位:符号为,常用的单位为(或)
3、表达式为:
注:表达式中nB表示,V表示,CB表示
学点二一定物质的量浓度的溶液的配制1、配置100ml0
4mol/l的NaCl溶液主要仪器有、、、、、等
注:(1)容量瓶的有一定规格,在使用时要注意标明;(2)容量瓶上标有、、
2、配置步骤(1)计算:根据nB=CB·V可知n(NaCl)=,则m(NaCl)=g
(2)称量:用准确称取NaCl固体
(3)溶解:将称好NaCl固体放入中,用适量蒸馏水溶解,用搅拌,并冷却至室温
(4)移液:将烧杯中的溶液用引流转移到中
(5)洗涤:用蒸馏水洗涤烧杯和玻璃棒次,并将洗涤液都转移入中,轻轻晃动,使溶液混合均匀
(6)定容:将蒸馏水注入容量瓶,当液面时,改用滴加蒸馏水至
(7)摇匀:盖好瓶塞,反复上下颠倒,摇匀
学点三溶液的稀释(1)稀释时,浓、稀溶液之间的关系式:c(浓溶液)·V(浓溶液)=c(稀溶液)·V(稀溶液)(2)在稀释浓溶液时,发生了变化,但溶液中保持不变
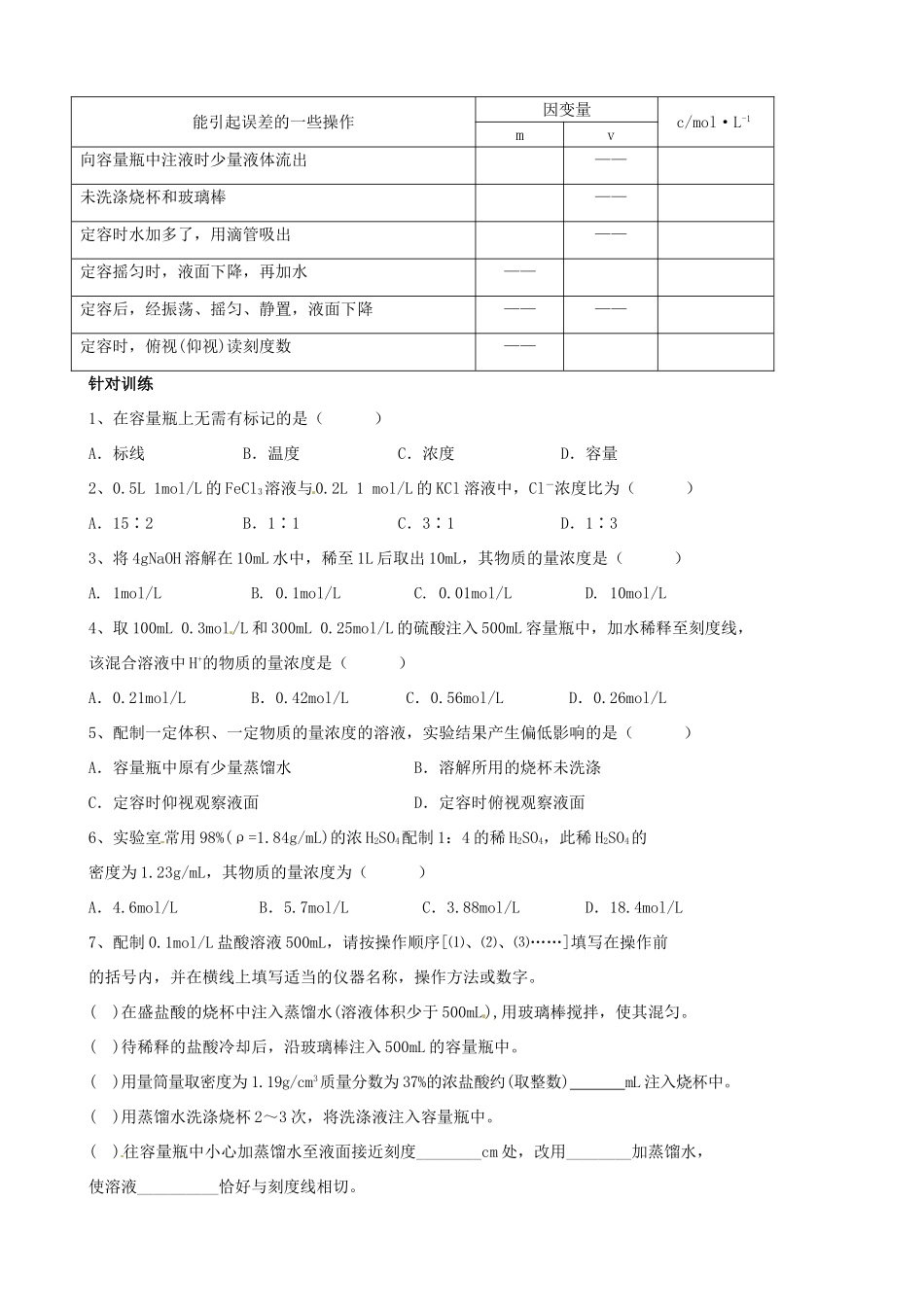
交流·研讨常见误差分析(前二栏填“增大”“减小”后一栏填“偏大”“偏小”“无影响”)能引起误差的一些操作因变量c/mol·L-1[mv向容量瓶中注液时少量液体流出——未洗涤烧杯和玻璃棒——定容时水加多了,用滴管吸出——定容摇匀时,液面下降,再加水——定容后,经振荡、摇匀、静置,液面下降————定容时,俯视(仰视)读刻度数——针对训练1、在容量瓶上无需有标记的是()A.标线