西南师大附中2010—2011学年度上期期末考试高一化学试题(总分:150分考试时间:120分钟)注意事项:1.答卷前考生务必将自己的班级、姓名、考号和考试科目填在答题卡上
2.第I卷每小题选出答案后,用铅笔把答题卡上对应题目的答案标号涂黑,如需改动,用橡皮擦干净后,再选涂其它答案,不能答在试题卷上
3.第II卷必须使用0
5毫米的黑色签字笔书写在答题卡上
4.考试结束,将答题卡上交(第I、II卷自己保管好,以备评讲)第Ⅰ卷选择题(共72分)相对原子质量:H1He4C12N14O16Na23F19Al27Cl35
5K39Fe56Cu64一、选择题(共18小题,每小题4分,共72分
每题只有一个选项符合题意
)1.化学与科学、技术、社会、环境密切相关
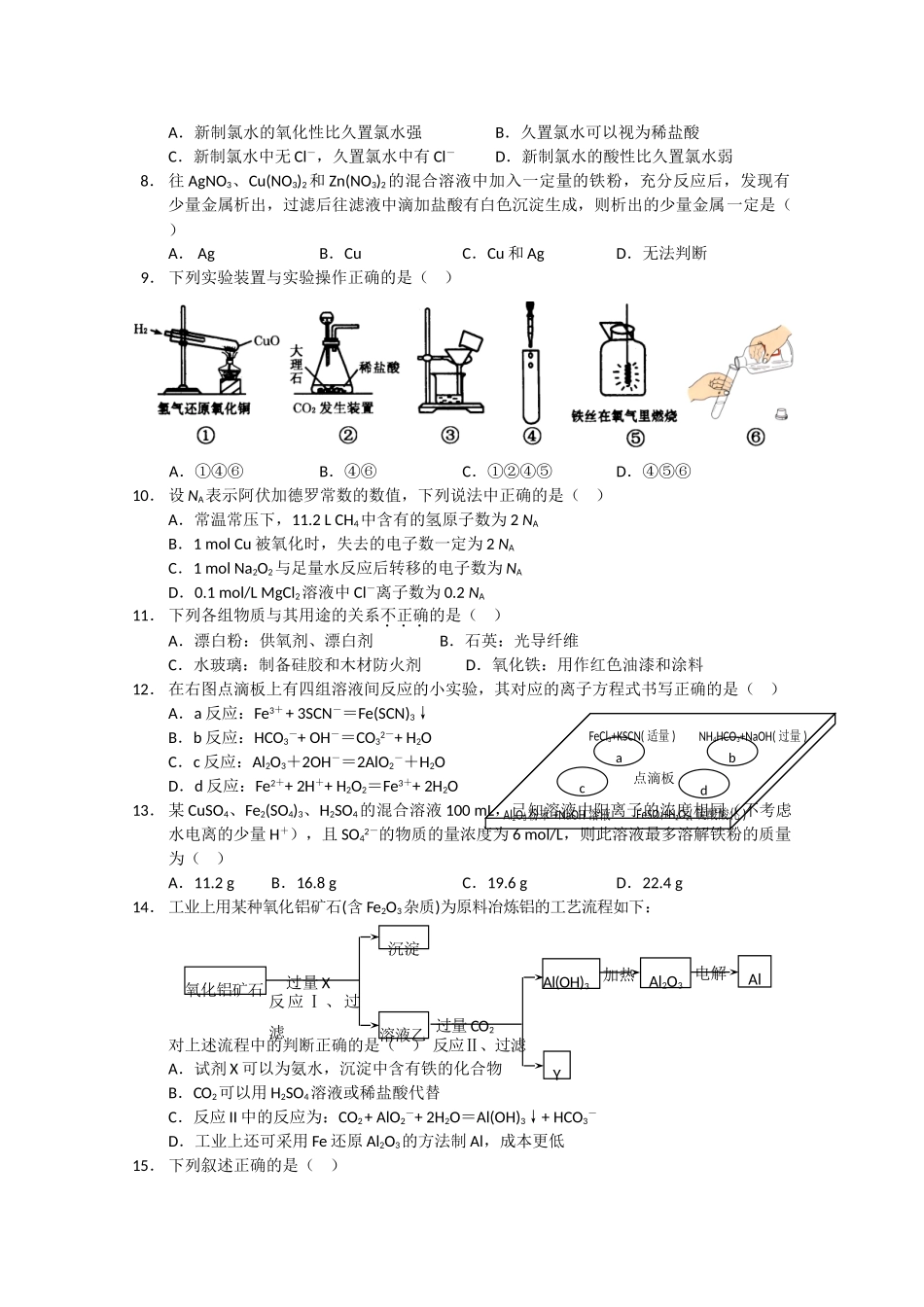
下列有关说法中错误的是()A.为防止中秋月饼等富脂食品因被氧化而变质,常在包装袋中放入生石灰或硅胶B.小苏打是制作馒头和面包等糕点的膨松剂,还是治疗胃酸过多的一种药剂C.2010年11月广州亚运会燃放的焰火是某些金属元素焰色反应所呈现出来的色彩D.青铜是我国使用最早的合金材料,目前世界上使用量最大的合金材料是钢铁2.下列说法正确的是()A.被氧化的物质是氧化剂B.可以利用酒精将碘水中的碘提取出来C.化合反应一定不是氧化还原反应D.铝抗腐蚀是外层氧化膜致密的缘故3.在水溶液中能大量共存,且加入过量的NaOH溶液时,有沉淀生成的是()A.K+、Ag+、NO3-、Cl-B.NH4+、Ba2+、Cl-、CO32-C.Na+、Ca2+、HCO3-、NO3-D.Na+、Al3+、SO42-、NO3-4.自然界里常见金属元素存在最多的是铝,其次是铁,铜的含量较少
然而人类冶炼金属获得成功最早的反而是含量少的铜,含量最多的铝最迟冶炼出来,究其原因,合理的是()A.铜矿较易还原,铝矿很难还原B.铜矿颜色较深,易发现;铝矿颜色较浅,不易发现C