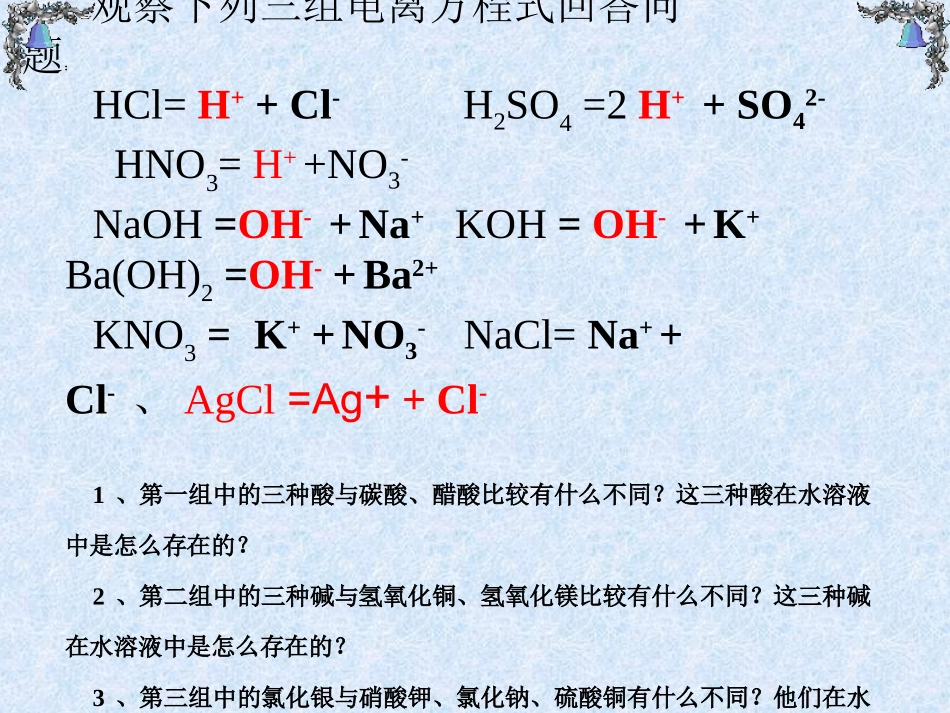
§2-2离子反应奇台农场中学张世君观察下列三组电离方程式回答问题:HCl=H++Cl-H2SO4=2H++SO42-HNO3=H++NO3-NaOH=OH-+Na+KOH=OH-+K+Ba(OH)2=OH-+Ba2+KNO3=K++NO3-NaCl=Na++Cl-、AgCl=Ag++Cl-1、第一组中的三种酸与碳酸、醋酸比较有什么不同
这三种酸在水溶液中是怎么存在的
2、第二组中的三种碱与氢氧化铜、氢氧化镁比较有什么不同
这三种碱在水溶液中是怎么存在的
3、第三组中的氯化银与硝酸钾、氯化钠、硫酸铜有什么不同
他们在水溶液中是怎么存在的
4、以上物质之间能发生的反应是我们初中学的哪种反应
若将100mL1mol·L-1KNO3溶液与100mL1mol·L-1NaCl溶液混合,求混合液中的离子种类及数目
若将100mL1mol·L-1AgNO3溶液与100mL1mol·L-1NaCl溶液混合,求混合液中的离子种类及数目
算一算第1种情况中,混合液里含有K+、NO3-、Na+、Cl-四种离子各0
1mol,说明这些离子在溶液中是共存的,相互之间没有反应;而第2种情况中,溶液里仅存在NO3-、Na+两种离子各0
1mol,原因是0
1molAg+与0
1molCl-恰好结合生成了难溶的AgCl沉淀总结归纳原来并不是所有的电解质溶液混合都会发生反应呀
向盛有5mLCuSO4溶液的试管中加入5mLNaCl溶液2
向盛有5mLCuSO4溶液的试管中加入5mLBaCl2溶液做一做,看一看离子反应的本质CuSO4+NaClCuSO4+BaCl2部分离子间发生反应Ba2++SO42-=BaSO4↓Cu2+SO42-Na+Cl-Cu2+SO42-Ba2+Cl-离子方程式:离子方程式的书写步骤写:写出正确的化学方程式((基础)拆:把易溶于水、易电离的物质(强酸、强碱、易溶盐)拆写成离子形式