实验一线性极化法测定金属Fe在稀H2SO4中的腐蚀速度一、基本要求1
掌握动电位扫描法测定电极极化曲线的原理和实验技术
通过测定Fe在0
1M硫酸溶液中的极化曲线,求算Fe的自腐蚀电位,自腐蚀电流
讨论极化曲线在金属腐蚀与防护中的应用
二、实验原理当金属浸于腐蚀介质时,如果金属的平衡电极电位低于介质中去极化剂(如H+或氧分子)的平衡电极电位,则金属和介质构成一个腐蚀体系,称为共轭体系
此时,金属发生阳极溶解,去极化剂发生还原
以金属铁在盐酸体系中为例:阳极反应:Fe-2e=Fe2+阴极反应:H++2e=H2阳极反应的电流密度以ia表示,阴极反应的速度以ik表示,当体系达到稳定时,即金属处于自腐蚀状态时,ia=ik=icorr(icorr为腐蚀电流),体系不会有净的电流积累,体系处于一稳定电位c
根据法拉第定律,体系通过的电流和电极上发生反应的物质的量存在严格的一一对应关系,故可阴阳极反应的电流密度代表阴阳极反应的腐蚀速度
金属自腐蚀状态的腐蚀电流密度即代表了金属的腐蚀速度
因此求得金属腐蚀电流即代表了金属的腐蚀速度
金属处于自腐蚀状态时,外测电流为零
极化电位与极化电流或极化电流密度之间的关系曲线称为极化曲线
极化曲线在金属腐蚀研究中有重要的意义
测量腐蚀体系的阴阳极极化曲线可以揭示腐蚀的控制因素及缓蚀剂的作用机理
在腐蚀点位附近积弱极化区的举行集会测量可以可以快速求得腐蚀速度
还可以通过极化曲线的测量获得阴极保护和阳极保护的主要参数
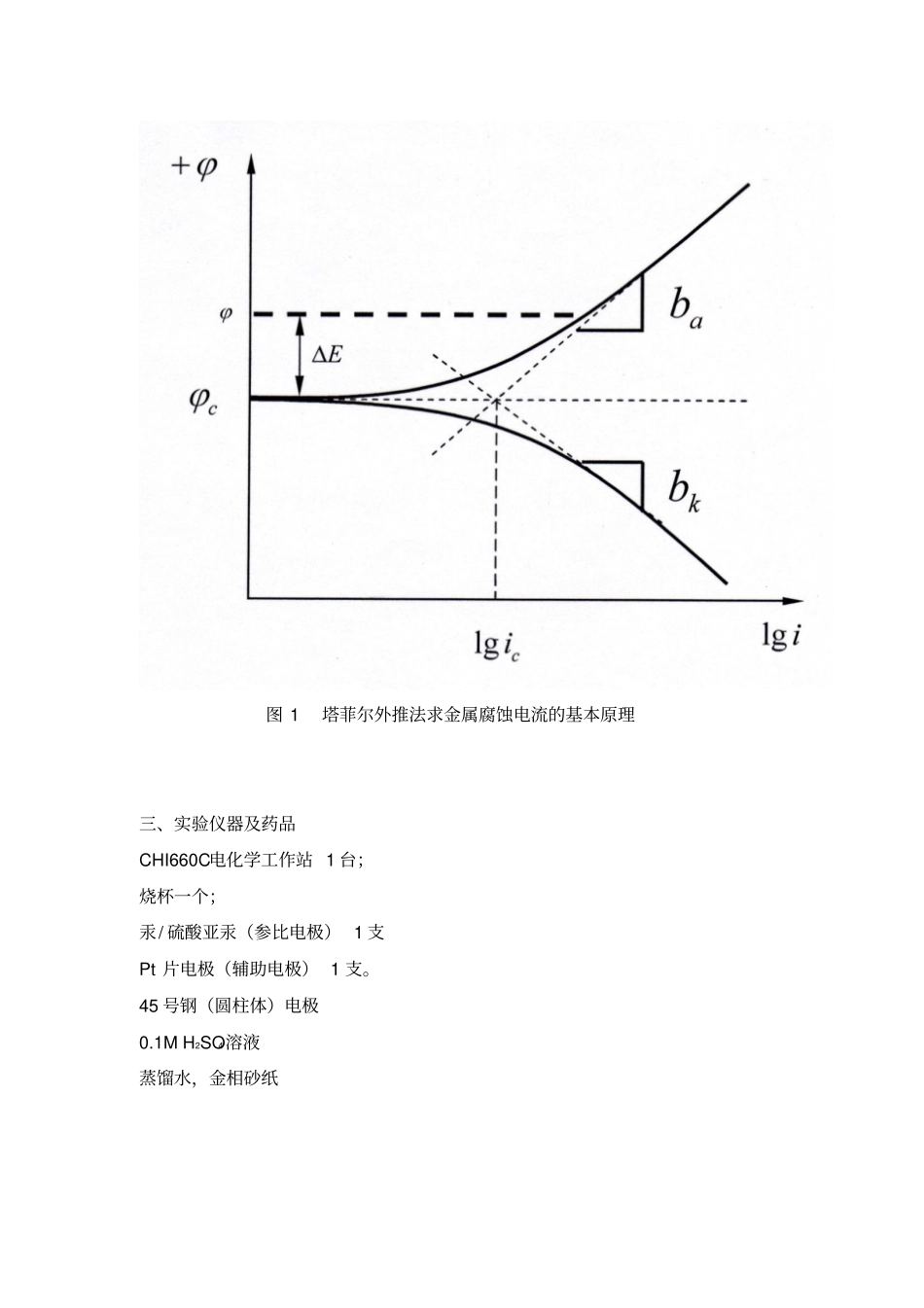
在活化极化控制下,金属腐蚀速度的一般方程式为:其中I为外测电流密度,ia为金属阳极溶解的速度,ik为去极化剂还原的速度,βa、βk分别为金属阳极溶解的自然对数塔菲尔斜率和去极化剂还原的自然对数)]exp()[exp(kcaccorrkaiiiI塔菲尔斜率
若以十为底的对数,则表示为ba、bk
这就是腐蚀金属电极的极化曲线方程式,令