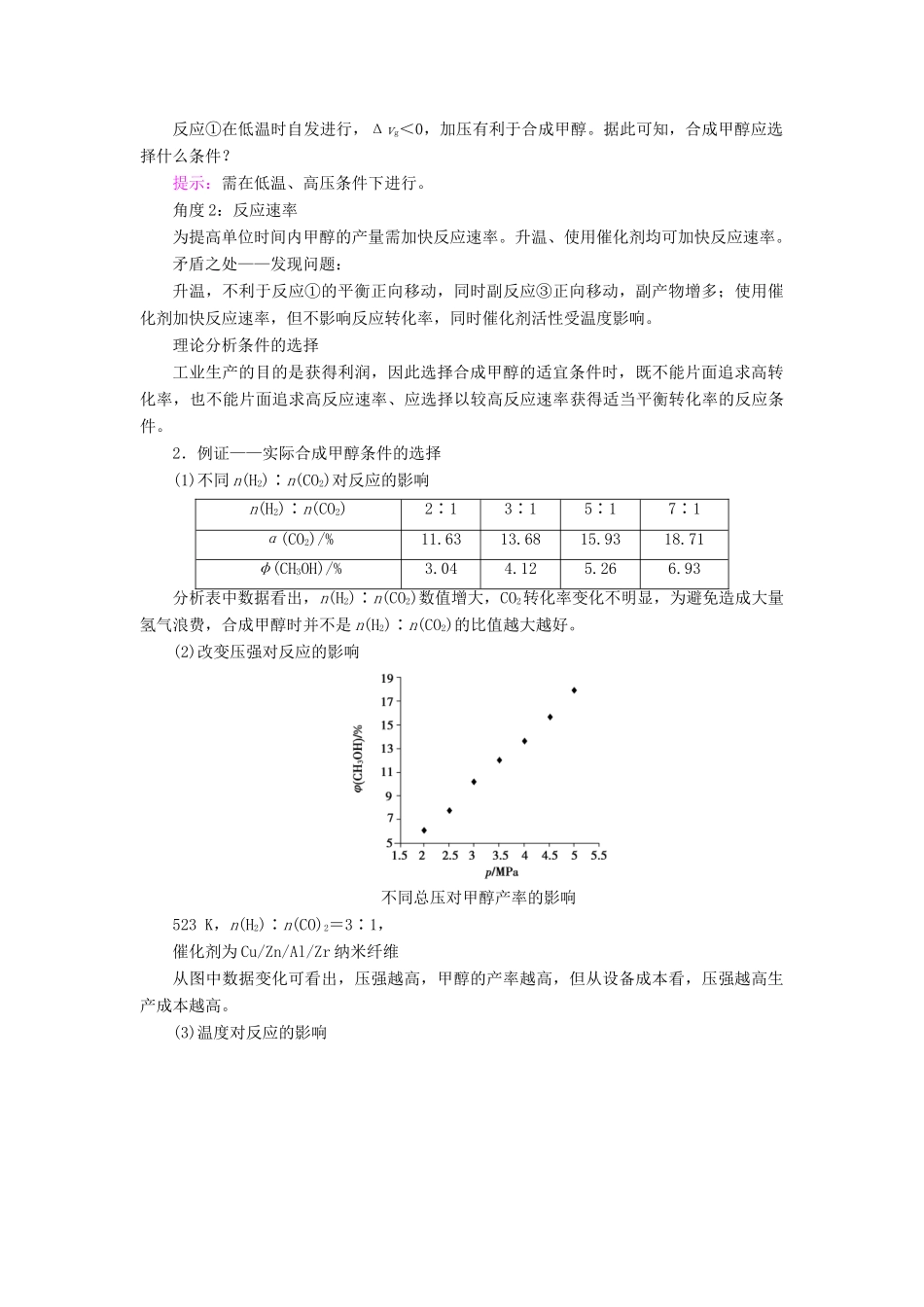
微项目探讨如何利用工业废气中的二氧化碳合成甲醇——化学反应选择与反应条件优化通过利用工业废气中的二氧化碳合成甲醇反应的选择以及对反应条件的优化,体会反应的焓变、熵变、化学平衡和速率相关知识的应用价值,形成从物质转化以及反应的方向、限度、快慢等多个角度综合分析、解决工业生产实际问题的基本思路
通过本项目的学习,树立绿色化学理念,认识到利用化学反应将无用物质转化为有用物质是解决环境问题的重要途径之一
[必备知识]1.目前有机原料按消费量排序,前4位从大到小依次是乙烯、丙烯、苯、甲醇
2.合成甲醇的原料3.选择CO2作碳源合成甲醇的原因(1)工业废气中含大量CO2,排放到空气中会带来环境问题;(2)天然气、煤、石油属于不可再生资源,日渐减少;(3)用CO2合成甲醇符合绿色化学要求
项目活动1选择合适的化学反应假设反应焓变和熵变不随温度的改变而变化,已知298K,100kPa时,有如下反应:①CO2(g)+3H2(g)===CH3OH(g)+H2O(g)ΔH=-48
97kJ·mol-1ΔS=-177
16J·mol-1·K-1②CO2(g)+2H2O(g)===CH3OH(g)+O2(g)ΔH=+676
48kJ·mol-1ΔS=-43
87J·mol-1·K-1③CO2(g)+H2(g)===CO(g)+H2O(g)ΔH=+41
17kJ·mol-1ΔS=+42
08J·mol-1·K-1[思考]1.请根据焓变和熵变复合判据判断上述三个反应是否正向自发进行
提示:反应①,ΔH-TΔS=-48
97kJ·mol-1-298K×(-0
17716)kJ·mol-1·K-1≈3
82kJ·mol-1>0,该反应属于放热熵减反应,降低温度时正向反应自发进行
反应②,ΔH-TΔS=+676
48kJ·mol-1-298K×(-0
04387)kJ·mol-1·K-1≈+689