氨与铵态氮肥[核心素养发展目标]1
通过实验知道氨的溶解性、氨与水和酸的反应
通过分析化合价认识氨的还原性
通过实验,知道铵盐的性质、NH的检验以及氨的实验室制法
一、氨的性质1
物理性质颜色气味密度溶解性沸点无色刺激性气味小于空气极易溶于水较低,易液化2
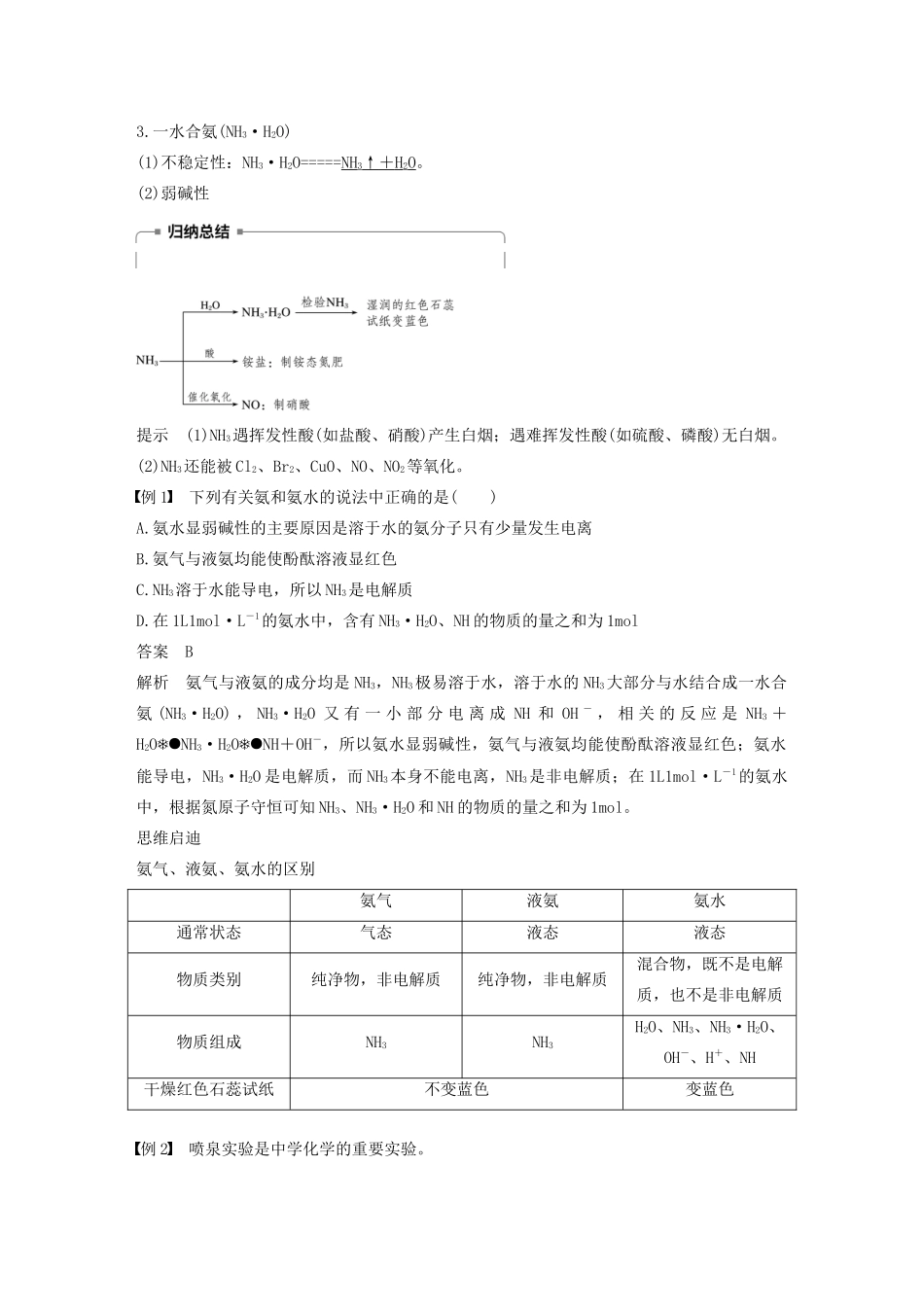
化学性质(1)与水反应——喷泉实验:实验装置操作及现象结论方程式打开止水夹,并挤压滴管的胶头;烧杯中的溶液由玻璃管进入圆底烧瓶,形成喷泉,瓶内液体呈红色氨易溶于水,水溶液呈碱性NH3+H2ONH3·H2O,NH3·H2ONH+OH-(2)与酸反应①与盐酸反应:实验实验现象结论方程式抽去玻璃片,集气瓶中产生白烟NH3和HCl反应生成NH4ClNH3+HCl===NH4Cl当蘸浓盐酸的玻璃棒与蘸浓氨水的玻璃棒靠近时也有白烟产生
②与硫酸反应化学方程式:2NH3+H2SO4===(NH4)2SO4或NH3+H2SO4===NH4HSO4
(3)与氧气反应NH3分子中氮元素的化合价为-3价,因此氨具有还原性
请写出氨气与氧气在催化剂作用下生成NO的化学方程式:4NH3+5O2=====4NO+6H2O
一水合氨(NH3·H2O)(1)不稳定性:NH3·H2O=====NH3↑+H2O
(2)弱碱性提示(1)NH3遇挥发性酸(如盐酸、硝酸)产生白烟;遇难挥发性酸(如硫酸、磷酸)无白烟
(2)NH3还能被Cl2、Br2、CuO、NO、NO2等氧化
例1下列有关氨和氨水的说法中正确的是()A
氨水显弱碱性的主要原因是溶于水的氨分子只有少量发生电离B
氨气与液氨均能使酚酞溶液显红色C
NH3溶于水能导电,所以NH3是电解质D
在1L1mol·L-1的氨水中,含有NH3·H2O、NH的物质的量之和为1mol答案B解析氨气与液氨的成分均是NH3,NH3极易溶于水,溶于水的NH3大部分与水结合成一水合氨(NH3·H2O),