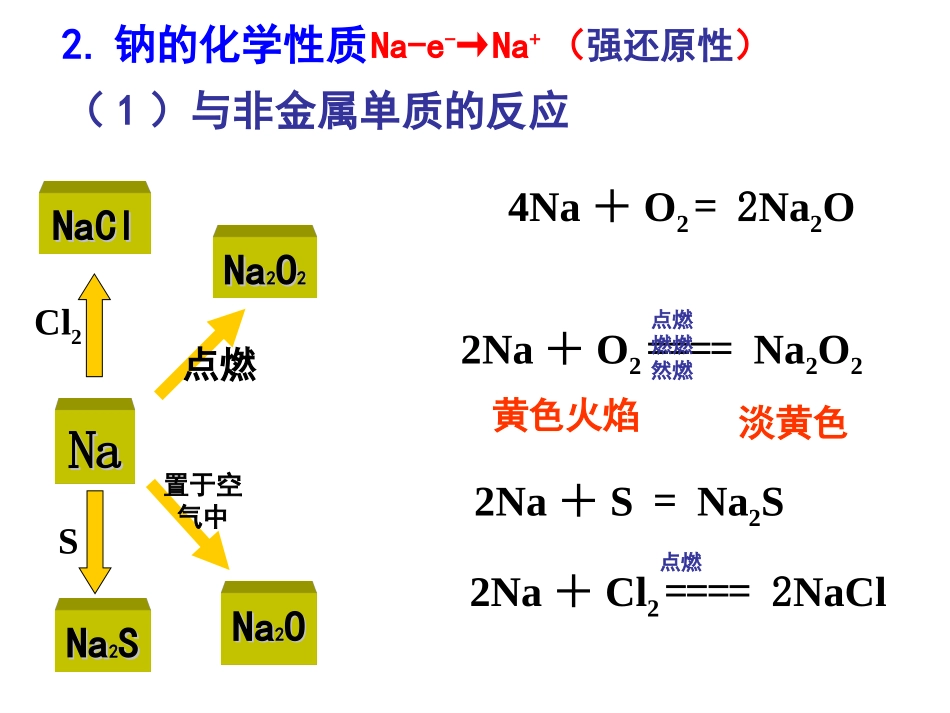
第一节第一节金属钠及其化合物金属钠及其化合物白:银白色、具有光泽,固体软:硬度小,很软[易切开、轻压变形]轻:密度小,0.97g/cm3[介于水和煤油之间]低:熔点:97.81℃、沸点:882.9℃[低]导:热和电的良导体(原子反应堆的导热剂)1.钠的物理性质:一、金属钠五字诀:“白、软、轻、低、导”五字诀:“白、软、轻、低、导”2.钠的化学性质NaNa22SSNaNaNaNa22OO22NaClNaClNaNa22OO淡黄色Cl2点燃置于空气中S2Na+O2====Na2O2点燃燃燃然燃4Na+O2=2Na2O2Na+S=Na2S2Na+Cl2====2NaCl点燃(1)与非金属单质的反应Na-e-→Na+(强还原性)黄色火焰Na浮在水面上,到处游动,熔成闪亮的小球,发出嘶嘶的响声,滴入酚酞后变红。2C2H5OH+2Na2C2H5ONa+H2↑2Na+2H2O=2NaOH+H2↑2CH3COOH+2Na2CH3COONa+H2↑(3)与稀酸溶液的反应2Na+2HCl=2NaCl+H2↑(4)与某些盐的反应4Na+TiCl4===4NaCl+Ti熔融((22)与水、与醇、酚、羧酸等含-)与水、与醇、酚、羧酸等含-OHOH的有机物反应的有机物反应钠与水反应的现象:钠与水反应的现象:(5)与盐溶液的反应(先与水,产物再与盐反应)浮、熔、游、响、红浮、熔、游、响、红思考:思考:把一小块金属钠分别投入饱和把一小块金属钠分别投入饱和NaClNaCl溶液、溶液、NHNH44ClCl溶液、溶液、CuSOCuSO44溶液的烧杯里的现象和反应溶液的烧杯里的现象和反应现象现象化学方程式化学方程式饱和饱和NaClNaCl饱和饱和NHNH44ClClCuSOCuSO44溶液溶液钠消失,放出无色无钠消失,放出无色无味气体、味气体、析出晶体析出晶体2Na+2H2Na+2H22O=2NaOH+HO=2NaOH+H22↑↑钠钠消失消失,有刺激性气,有刺激性气味气体放出味气体放出钠钠消失消失,放出无色无,放出无色无味气体,有味气体,有蓝色沉淀蓝色沉淀2Na+2H2Na+2H22O+CuSOO+CuSO44==NaNa22SOSO44+H+H22↑+Cu(OH)↑+Cu(OH)22↓↓2Na+2NH2Na+2NH44ClCl=2NaCl+H=2NaCl+H22↑+2NH↑+2NH33↑↑把一大块钠投入少量把一大块钠投入少量AlClAlCl33溶液中呢?溶液中呢?3.钠的存在、制备和用途。存在:2NaCl===2Na+Cl2↑电解熔融制备:用途:只以化合态存在(1)制Na2O2(2)制Na-K合金,原子反应堆导热剂(3)高压钠灯(4)还原贵金属(和氧气反应)(钠的导热性)(黄光射程远,透雾力强)(钠具有强还原性)钠灯4、焰色反应1、原理:某些金属或其化合物灼烧时使火焰呈现出特殊的颜色。2、操作:把铂丝用盐酸洗涤后灼烧,反复多次,至火焰变为无色。用干净的铂丝蘸一些溶液,放到酒精灯火焰上灼烧。3、应用:(1)离子检验,物质鉴别。钠(黄色)、钾(紫色,透过蓝色钴玻璃)(2)焰火材料。练一练练一练1.1.一块表面已氧化成氧化钠的钠块一块表面已氧化成氧化钠的钠块5.4g5.4g投入足量的水中,投入足量的水中,最多能产生最多能产生0.1g0.1g气体,则原来被氧化的钠的质量是气体,则原来被氧化的钠的质量是()()AA、、2.3gB2.3gB、、3.1gC3.1gC、、4.6gD4.6gD、、5.3g5.3gAA2.2.钠露置在空气中的最终产物是什么?钠露置在空气中的最终产物是什么?表面变成溶液表面变成溶液((NaOHNaOH潮潮解)解)出现白色固体出现白色固体((NaOHNaOH))表面变暗表面变暗((NaNa22OO))银白色金属钠银白色金属钠((NaNa))白色粉末白色粉末((NaNa22COCO33))出现白色固体出现白色固体((NaNa22COCO33·10H·10H22OO))→→→→→→→→→→主题二、钠的氧化物☺Na2O与Na2O2的差异1.颜色差异:2.结构差异:3.氧元素价态差异:4.稳定性差异:Na2O为白色固体,Na2O2为淡黄色固体Na2O和Na2O2都为离子化合物,但Na2O中含有O2-,而Na2O2中含有O22-(过氧根离子)Na2O不稳定,能继续与氧气反应生成Na2O2,Na2O2比较稳定Na2ONa2O2-2-15.属类差异:①与水反应:②与CO2反应:③与酸的反应:对比以上反应,主要有二方面差异:①反应产物差异,Na2O2参加的反应中有O2产生;②反应类型差异,Na2O参与的反应为非氧化还原反应。Na2O属于碱性氧化物,Na2O2则属于过氧化物6.化学性质差异:Na2O+H2O=2NaOH2Na2O2+2H2O=4NaOH+O2↑Na2O+CO2=Na2CO32Na2O2+2CO2=2Na2CO3+O2↑Na2O+2HCl=2NaCl+H2O2Na2O2+4HCl=4NaCl+2H2O+O2↑呼吸面具呼吸面具中氧气...