第3讲电解池金属的电化学腐蚀与防护[考纲解读]1
了解电解池的工作原理,能写出电极反应和电池反应方程式
理解金属发生电化学腐蚀的原因、金属腐蚀的危害、防止金属腐蚀的措施
考点一电解的原理1.电解定义在________作用下,电解质在两个电极上分别发生______和__________的过程
2.能量转化形式________转化为________
3.电解池(1)构成条件①有与________相连的两个电极
②__________(或__________)
③形成____________
(2)电极名称及电极反应(如图)(3)电子和离子移动方向①电子:从电源________流向电解池的________;从电解池的________流向电源的________
②离子:阳离子移向电解池的________;阴离子移向电解池的________
4.分析电解过程的思维程序(1)首先判断阴、阳极,分析阳极材料是惰性电极还是活泼电极
(2)再分析电解质水溶液的组成,找全离子并分阴、阳两组(不要忘记水溶液中的H+和OH-)
(3)然后排出阴、阳两极的放电顺序阴极:阳离子放电顺序:Ag+>Fe3+>Cu2+>H+(酸)>Fe2+>Zn2+>H+(水)>Al3+>Mg2+>Na+>Ca2+>K+
阳极:活泼电极>S2->I->Br->Cl->OH->含氧酸根离子
(4)分析电极反应,判断电极产物,写出电极反应式,要注意遵循原子守恒和电荷守恒
(5)最后合并两个电极反应式得出电解反应的总化学方程式或离子方程式
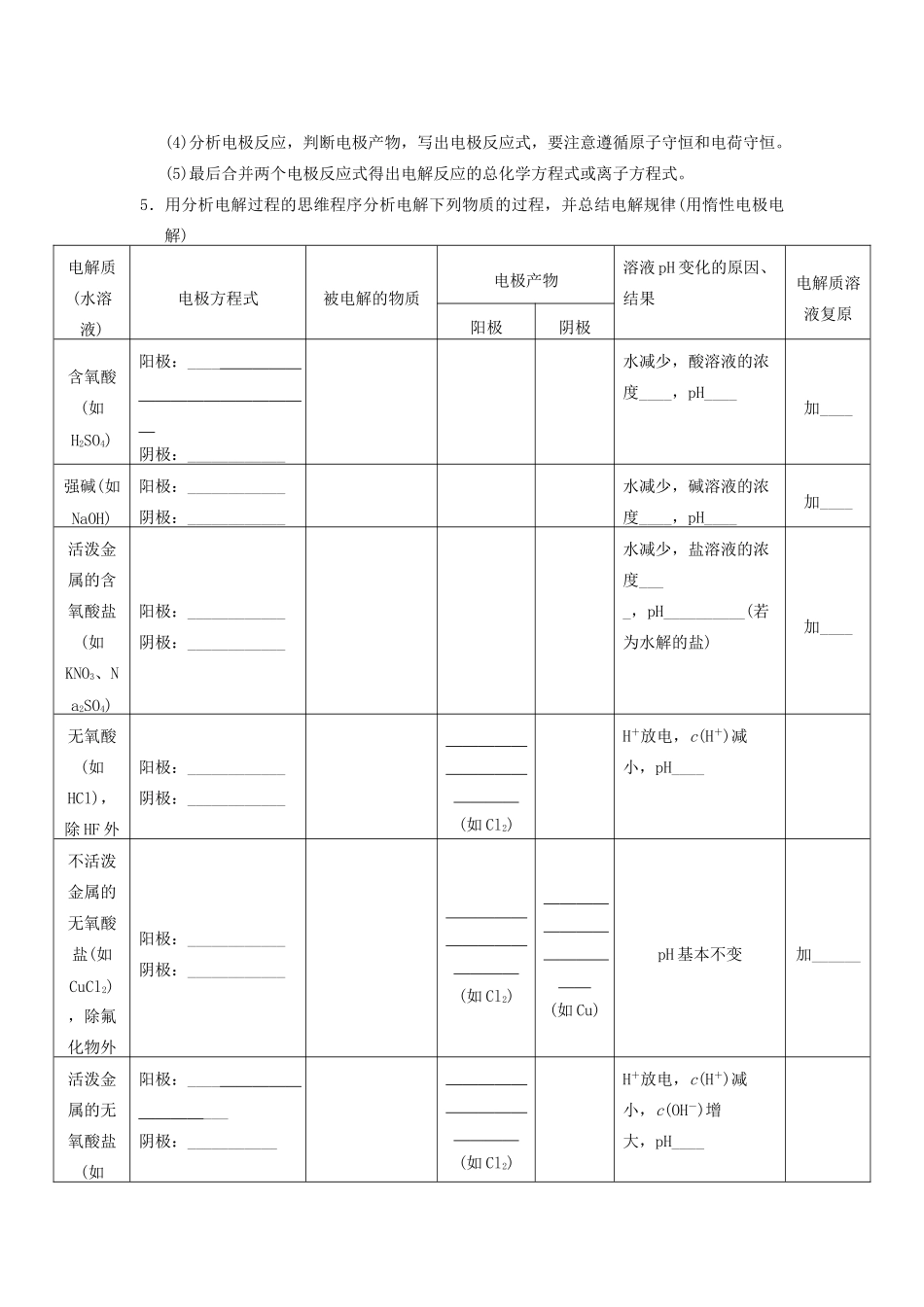
5.用分析电解过程的思维程序分析电解下列物质的过程,并总结电解规律(用惰性电极电解)电解质(水溶液)电极方程式被电解的物质电极产物溶液pH变化的原因、结果电解质溶液复原阳极阴极含氧酸(如H2SO4)阳极:____阴极:____________水减少,酸溶液的浓度____,pH____加__