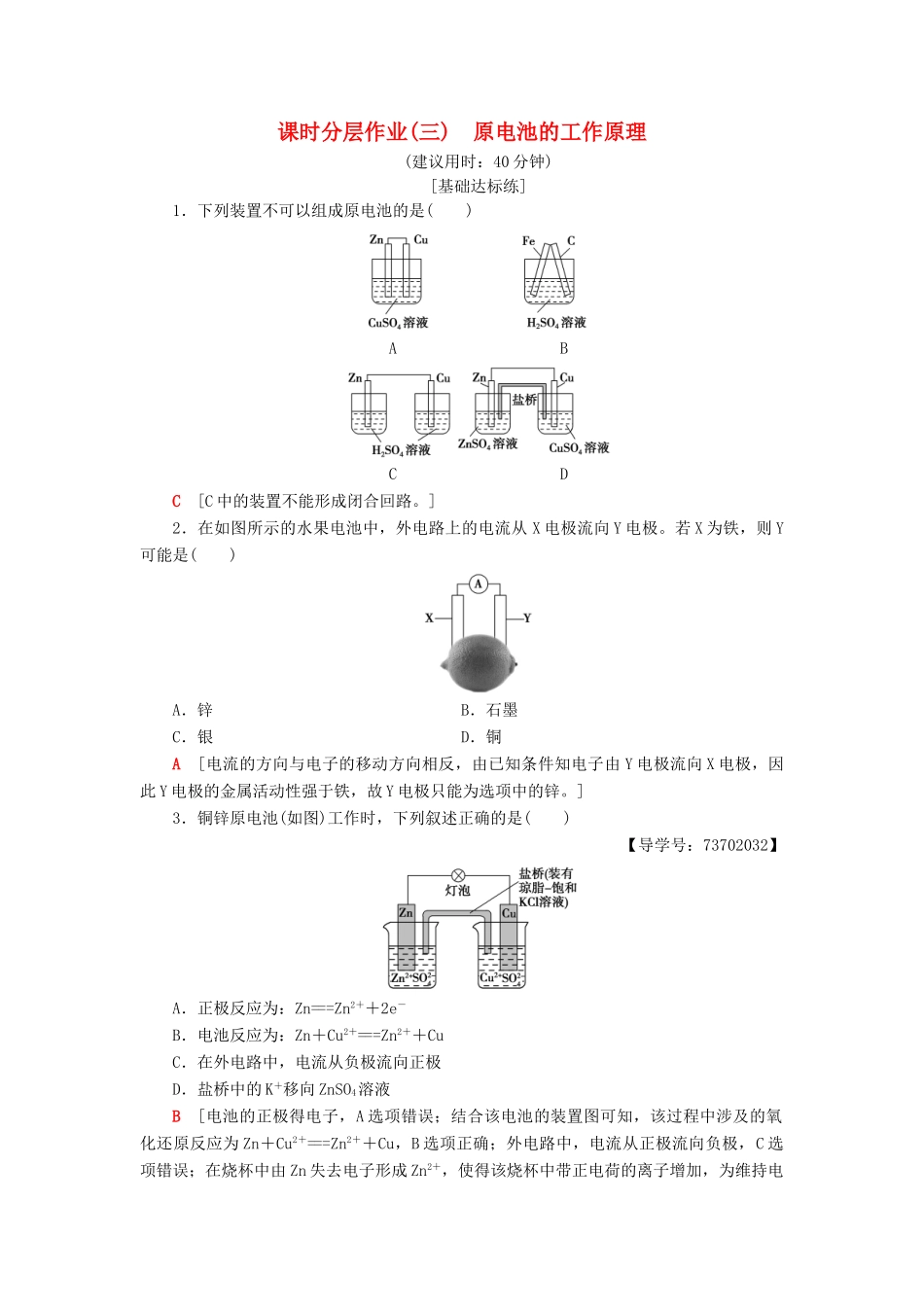
课时分层作业(三)原电池的工作原理(建议用时:40分钟)[基础达标练]1.下列装置不可以组成原电池的是()ABCDC[C中的装置不能形成闭合回路
]2.在如图所示的水果电池中,外电路上的电流从X电极流向Y电极
若X为铁,则Y可能是()A.锌B.石墨C.银D.铜A[电流的方向与电子的移动方向相反,由已知条件知电子由Y电极流向X电极,因此Y电极的金属活动性强于铁,故Y电极只能为选项中的锌
]3.铜锌原电池(如图)工作时,下列叙述正确的是()【导学号:73702032】A.正极反应为:Zn===Zn2++2e-B.电池反应为:Zn+Cu2+===Zn2++CuC.在外电路中,电流从负极流向正极D.盐桥中的K+移向ZnSO4溶液B[电池的正极得电子,A选项错误;结合该电池的装置图可知,该过程中涉及的氧化还原反应为Zn+Cu2+===Zn2++Cu,B选项正确;外电路中,电流从正极流向负极,C选项错误;在烧杯中由Zn失去电子形成Zn2+,使得该烧杯中带正电荷的离子增加,为维持电中性,盐桥中的Cl-移向ZnSO4溶液,而K+应该通过盐桥流向CuSO4溶液所在的右烧杯,D选项错误
]4.关于原电池的说法,正确的是()A.在正极上发生氧化反应B.某电极上有氢气产生,则此电极为正极C.在外电路电子流出的为正极D.在负极上发生还原反应B[A项,正极发生还原反应;B项,产生H2的电极上得电子,发生还原反应,是正极;C项,外电路中电子由负极流出;D项,负极失去电子发生氧化反应
]5.某原电池反应为Fe+2Fe3+===3Fe2+,与此电池反应不符的原电池是()A.铜片、铁片、FeCl3溶液组成的原电池B.石墨、铁片、Fe(NO3)3溶液组成的原电池C.铁片、锌片、Fe2(SO4)3溶液组成的原电池D.银片、铁片、Fe(NO3)3溶液组成的原电池C[解答此题可采用逆向思维的方法,首先通过电池反应可知