受试者姓名拼音缩写□□□□封面阿美宁病例报告表(CaseReportForm)受试者姓名:家庭地址:联系电话:试验中心名称:申办单位:江苏豪森药业股份有限公司在正式填表前请认真阅读下列填表说明病例报告表填写说明:1.筛选合格者填写病例报告表
2.病例报告表填写务必准确、清晰,不得任意涂改,错误之处纠正时需用横线居中化出,并签署修改者姓名缩写及修改时间
3.填写记录一律用钢笔或碳素签字笔
4.患者姓名拼音缩写四个需填满,两字姓名填写两字拼音前两个字母;三字姓名填写三字首字母及第三字第二字母;四字姓名填写每个字的首字母
5.表中凡有“□”的项,请在符合的条目上划“√”
表格中所有栏目均应填写相应的文字或数字,不得留空
6.所有检验项目因故未查或漏查,请填写ND;具体合并用药剂量和时间不明,请先写NK
7.试验期间应如实填写合并用药记录表、不良事件记录表
记录不良事件的发生时间、严重程度、持续时间、采取的措施和转归
如有严重不良事件发生(包括临床验证过程中发生需住院治疗、延长住院时间、伤残、影响工作能力危及生命或死亡、导致先天畸形等事件),必须立即通知主要研究单位伦理委员会及申办单位
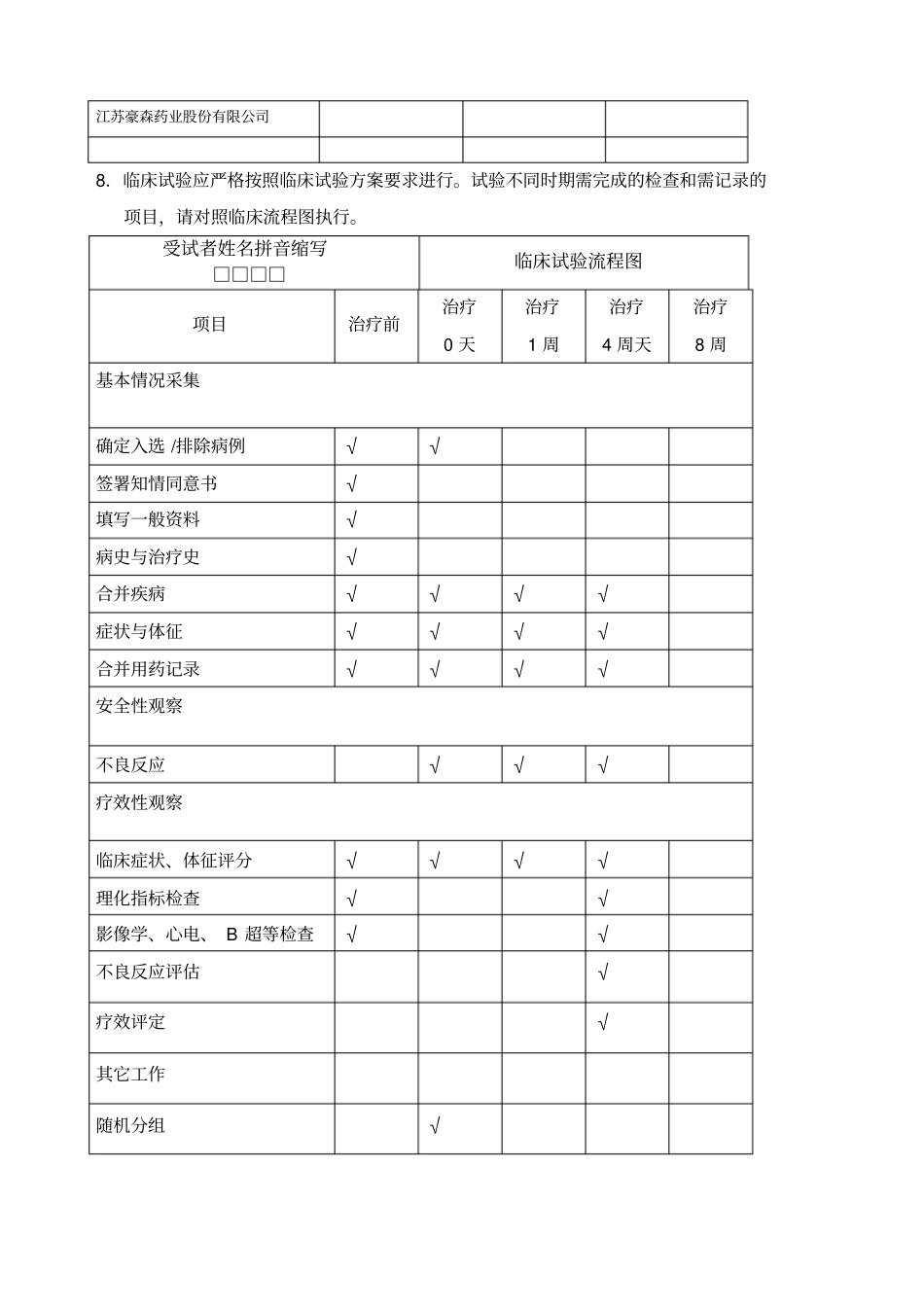
单位联系人联系电话传真江苏豪森药业股份有限公司8.临床试验应严格按照临床试验方案要求进行
试验不同时期需完成的检查和需记录的项目,请对照临床流程图执行
受试者姓名拼音缩写□□□□临床试验流程图项目治疗前治疗0天治疗1周治疗4周天治疗8周基本情况采集确定入选/排除病例√√签署知情同意书√填写一般资料√病史与治疗史√合并疾病√√√√症状与体征√√√√合并用药记录√√√√安全性观察不良反应√√√疗效性观察临床症状、体征评分√√√√理化指标检查√√影像学、心电、B超等检查√√不良反应评估√疗效评定√其它工作随机分组√分发研究产品√回收研究产品数量√受试者姓名拼音缩写□□□□患者知情同意书受试者知情同意书敬爱