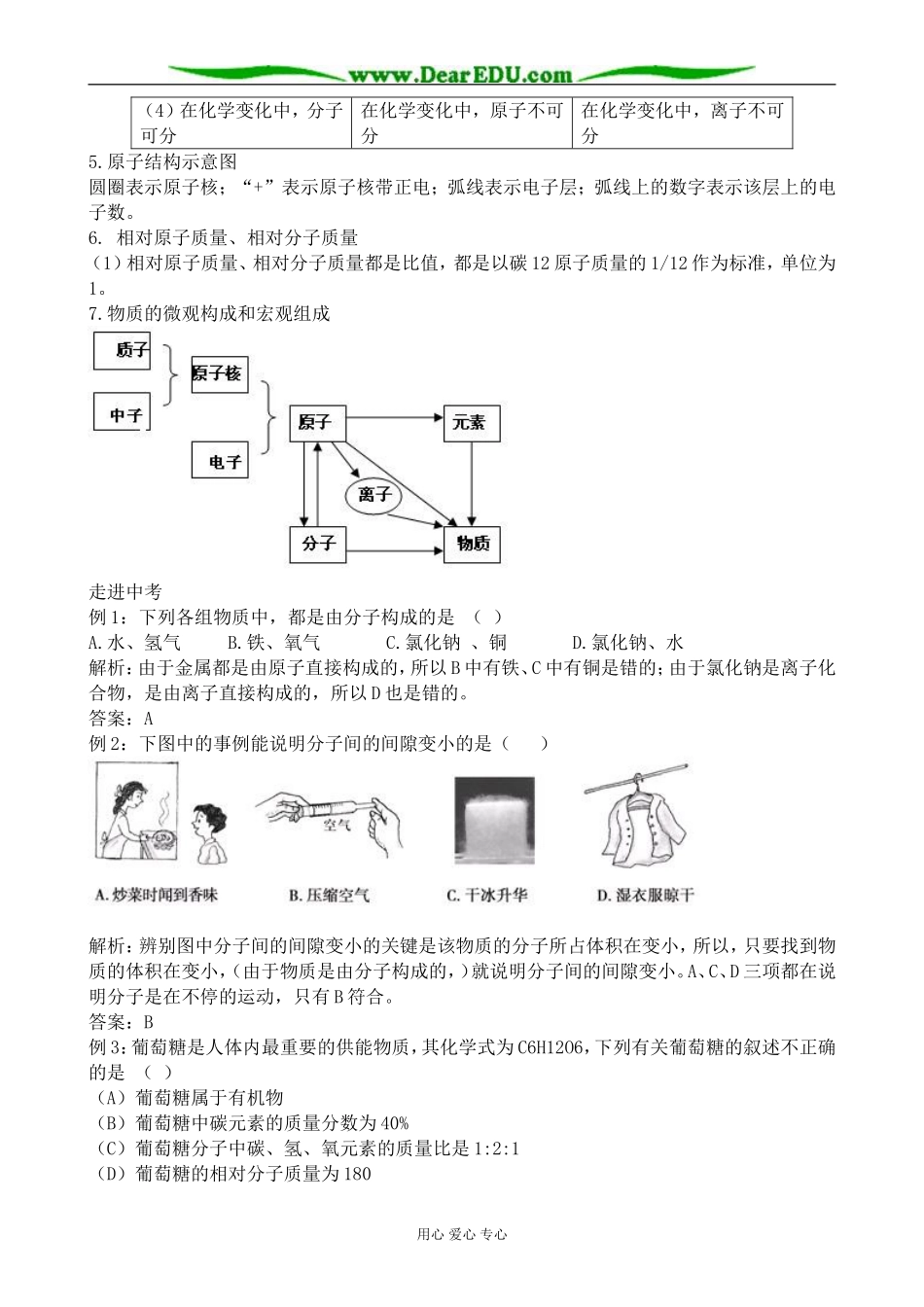
物质的组成和结构复习提要1
分子、原子分子:是保持物质化学性质的最小粒子
方法指导:(1)同种物质的分子性质相同,不同物质性质不同
例如,水分子是保持水化学性质的最小粒子,氧分子是保持氧气化学性质的最小粒子
空气中的氧气与实验室制取的氧气都是由氧分子构成的,它们的化学性质相同
(2)分子是构成物质的一种粒子
如:O2、H2O等
(3)分子的构成:由原子构成,其中同种元素的原子构成单质分子,不同种元素的原子构成化合物分子
如:O2、H2O等
(4)分子的性质:1
分子很小;2
分子在永不停息的作无规则运动;3
分子间有间隔
(5)分子与物质的变化:物质在发生物理变化时,分子本身不发生变化;物质在发生化学变化时,分子本身也发生变化
原子:是化学变化中的最小粒子
方法指导:(1)原子不可分只是在化学变化中,并不是不可分,原子是由原子核和电子构成的
(2)原子的结构:其中:核电荷数=质子数=核外电子数整个原子不显电性质子数决定着元素的种类;最外层电子数决定着元素的化学性质
(3)分子和原子的本质区别:在化学变化中分子可分,原子不可分
(4)原子也是构成物质的一种粒子
如:Fe、Mg、Al等都是由原子构成的
2.原子团记住几种常见的原子团:NO3、SO4、OH、CO3、NH43.离子离子:带电的原子或原子团
方法指导:(1)由于带电情况不同所以分为阴阳离子
(2)离子与原子的联系:原子得到电子→阴离子,原子失去电子→阳离子即:核电荷数=质子数=核外电子数±离子所带电荷数
(3)离子符号的书写:在元素符号的右上角写上该离子所带的电荷数,注意数字在前,电性在后
如:Ca2+、Al3+、Cl-、O2-4
分子、原子和离子的比较分子原子离子(1)能独立存在,并保持物质化学性质的最小粒子
能独立存在,是化学变化中的最小粒子
带电的原子或原子团
(2)用分子式表示
如:O2、H2O等