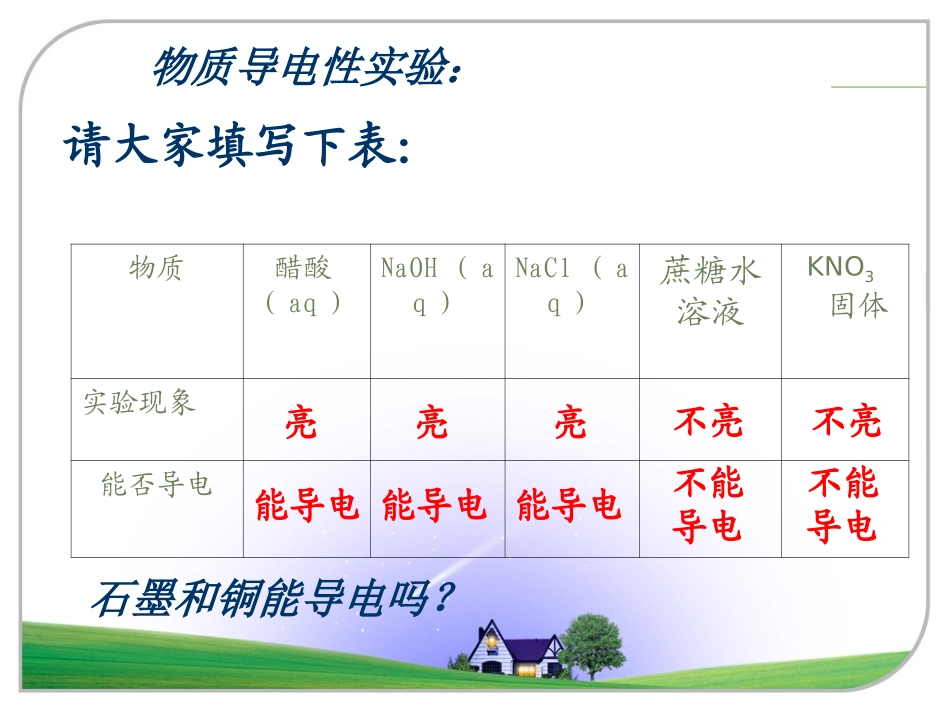
化学1许多化学反应是在水溶液中进行的第二节离子反应物质醋酸(aq)NaOH(aq)NaCl(aq)蔗糖水溶液KNO3固体实验现象能否导电请大家填写下表:不能导电不能导电能导电能导电能导电不亮亮亮亮不亮物质导电性实验:石墨和铜能导电吗
一、物质导电原因金属:自由移动的电子(石墨、Cu)溶液:电离出自由移动的离子(NaCl溶液、盐酸等)电离:指化合物在水溶液或熔融状态下产生自由移动的阴阳离子的过程
注意:固体中含离子,但不能自由移动(不导电)二、电解质与非电解质1、定义电解质:在水溶液或熔融状态下能导电的化合物(二者取其一)非电解质:在水溶液或熔融状态下都不能导电的化合物(二者同时都不能)注意事项:①均为化合物(混合物与单质既不是电解质,也不是非电解质)②指明条件:水溶液或熔融态导电电解质的水溶液电解质的熔融状态③自身电离的离子导电电解质如HCl、HNO3、CH3COOH等如NaOH、Ca(OH)2、Mg(OH)2等大多数盐水可溶性盐:如NaCl、KNO3等难溶性盐:如AgCl,BaSO4等如MgO、CaO等金属氧化物:酸:碱:2、范围非电解质非金属氧化物:CO2、NH3等大多数有机物:蔗糖、乙醇等思考:CO2、NH3在水溶液中能导电吗
判断下列物质哪些属于电解质,哪些属于非电解质①HCl②Ba(OH)2③NaCl④BaSO4⑤MgO⑥Cu⑦硫酸溶液⑧蔗糖⑨SO3提示:1
电解质要是化合物2
电解质要在水溶液或熔融状态下能导电电解质:非电解质:⑧②③④⑤⑨①盐酸和醋酸在水溶液中的电离
盐酸中存在盐酸中存在HH++、、ClCl--无无HClHCl分子分子醋酸溶液中存在醋酸溶液中存在HH++、、CHCH33COOCOO--和和CHCH33COOHCOOH分子分子三、强电解质与弱电解质(根据电离程度)强电解质:在水溶液中完全电离成离子的电解质
(离子)弱电解质:在水溶液中部分电离成