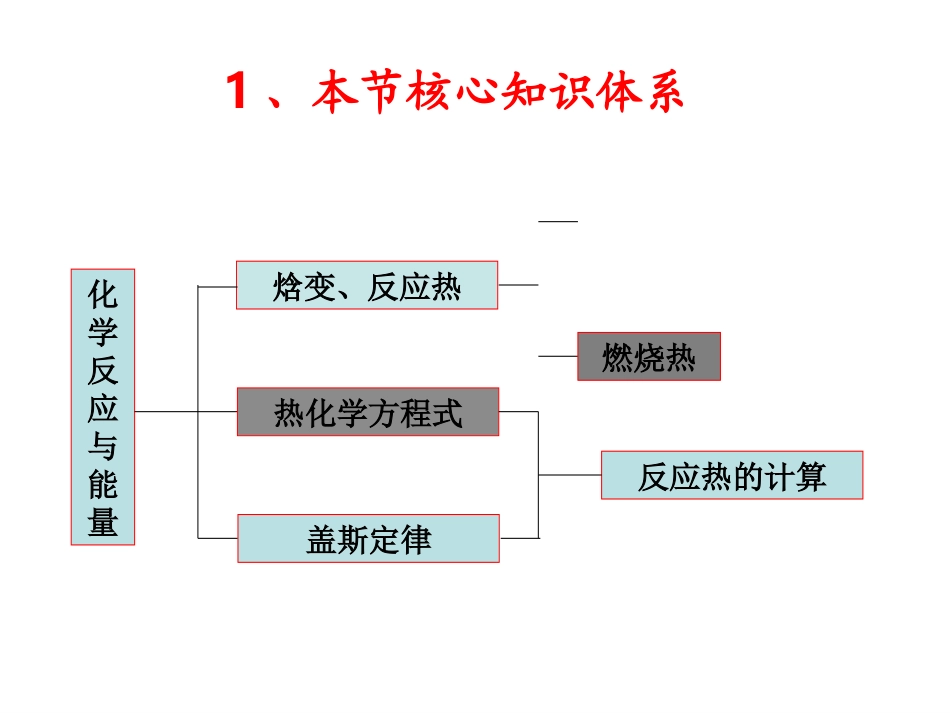
一、反应热、焓变1、反应热2、焓和焓变3、反应热和焓变复习回顾二、微观探究化学反应中能量变化的源泉四、用键能计算反应热三、放热反应和吸热反应与△H正负的关系1、本节核心知识体系化学反应与能量焓变、反应热热化学方程式盖斯定律反应热的计算燃烧热1、热化学方程式概念表示参加反应的物质的量和反应热的关系的化学方程式,叫做热化学方程式
能表示参加反应物质的量和反应热的关系的化学方程式H2(g)+I2(g)======2HI(g)△H=-14
9kJ/mol200℃101kPa1、热化学方程式包含物质变化和能量变化两个部分,二者缺一不可
普通化学方程式只包含物质变化一个部分
物质变化能量变化2、热化学方程式与普通化学反应的差异能表示参加反应物质的量和反应热的关系的化学方程式H2(g)+I2(g)======2HI(g)△H=-14
9kJ/mol200℃101kPa2、热化学方程式需注明反应时的温度和压强
对于25℃101kPa时进行的反应可不注明
普通化学方程式不需注明温度和压强
H2(g)+O2(g)==H2O(g)△H=-241
8kJ/mol122、热化学方程式与普通化学反应的差异能表示参加反应物质的量和反应热的关系的化学方程式3、热化学方程式需注明各物质的状态
普通化学方程式不需注明物质的状态
H2(g)+O2(g)==H2O(g)△H=-241
8kJ/mol12H2(g)+O2(g)==H2O(l)△H=-285
8kJ/mol122、热化学方程式与普通化学反应的差异能表示参加反应物质的量和反应热的关系的化学方程式4、热化学方程式中化学计量数表示参加反应的各物质的物质的量,可为整数或分数
普通化学方程式中化学计量数宏观上表示各物质的物质的量,微观上表示原子分子数目,只能为整数,不能为分数
H2(g)+O2(g)==H2O(g)△H=-241
8kJ/mol122H2(g)