第一节化学反应速率【学习目标】1.知道化学反应速率的定量表示方法,能进行有关化学反应速率的简单计算
2.了解测定化学反应速率的方法,通过实验测定某些化学反应的速率,结合实验培养观察、记录实验现象及数据处理能力
【活动过程】活动一:感知化学反应速率,了解测定化学反应速率的方法1.化学反应不同,反应速率也不相同
请你列举能体现化学反应速率快、慢的实例
2.实验探究反应速率快、慢的描述
⑴按右图安装两套装置,在锥形瓶内各盛有2g锌粒(颗粒大小基本相同),通过分液漏斗分别加入40mL1mol/L和40mL4mol/L的硫酸,比较二者收集10mLH2所用的时间,把实验结果填入下表:加入试剂反应时间/min反应速率/(mL·min-1)1mol/LH2SO44mol/LH2SO4理论上,我们还能通过哪些相关量的比较来描述反应速率的快慢
⑵事实上,化学反应中反应物和生成物的物质的量浓度、质量、体积、体系压强等相关的性质在测量反应速率时都可以加以利用
但有些物理量如物质的量浓度往往很难直接进行测量,必须依靠科学仪器才能测定
①对于有颜色变化的化学反应,科学家常常利用颜色的深浅对光的吸收程度不同来测量溶液中某物质的浓度变化
你认为这在科学上的依据是什么
②H+离子没有颜色,溶液中的H+离子浓度通常采用测导电性的方法(pH计的工作原理)来测定
其工作原理是什么
活动二:知道化学反应速率的定量表示方法1.你知道化学反应速率一般如何表示
其数学表达式怎样
常用单位是什么
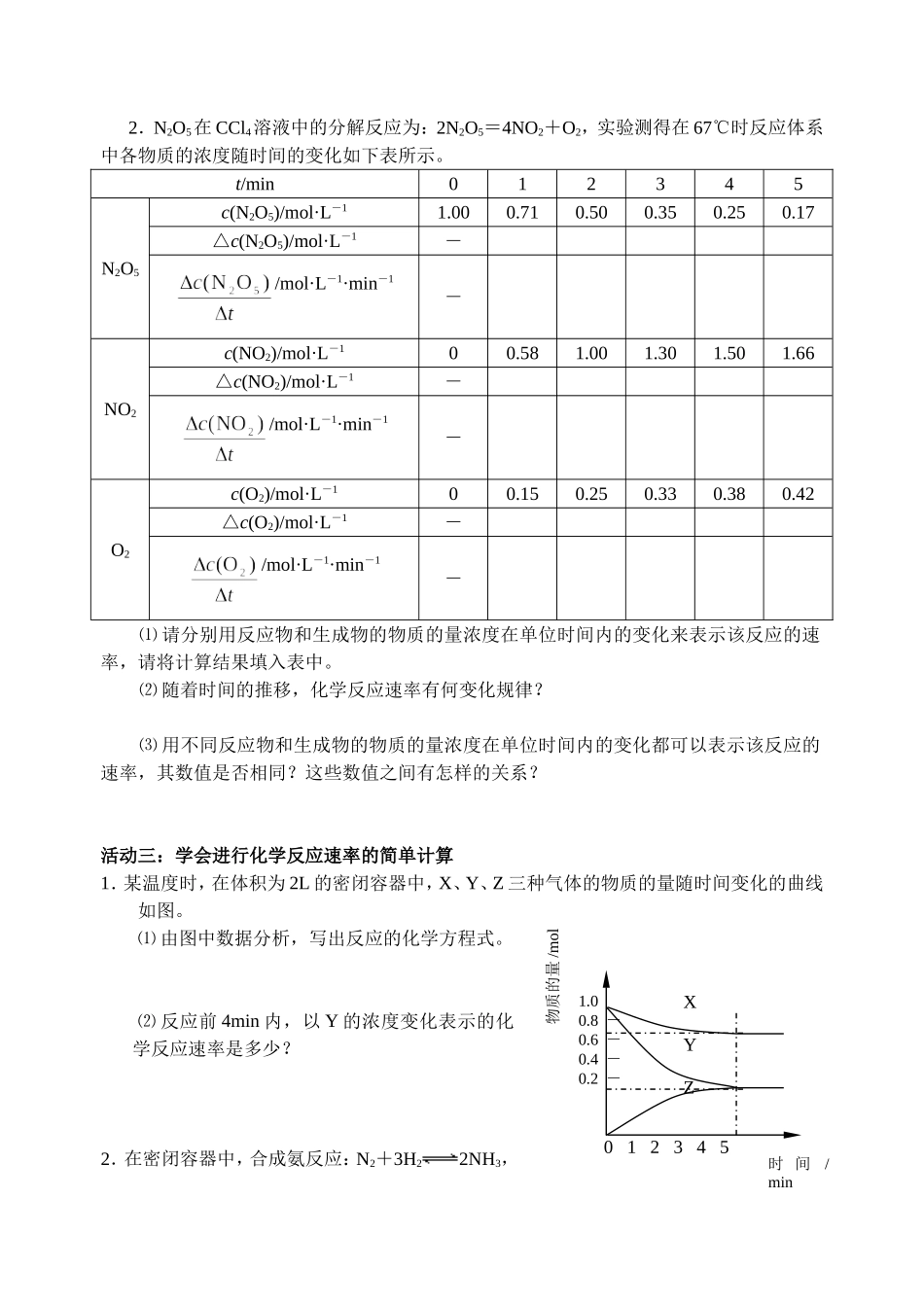
1020304050mLZn稀H2SO42.N2O5在CCl4溶液中的分解反应为:2N2O5=4NO2+O2,实验测得在67℃时反应体系中各物质的浓度随时间的变化如下表所示
t/min012345N2O5c(N2O5)/mol·L-11
17△c(N2O5)/mol·L-1-/mol·L-1