第二课时氯气的制法氯离子(Cl-)的检验课后提能·层级练1.欲除去Cl2中的少量HCl气体,可选用()A.NaOH溶液B.饱和食盐水C.浓硫酸D.石灰水解析:选B利用了HCl极易溶于水而Cl2在饱和食盐水中溶解度很小的原理
2.检验Cl-时所用试剂HNO3的作用是()A.防止CO的干扰B.防止Cl-的干扰C.生成Ag2CO3沉淀D.防止NO的干扰解析:选A检验Cl-加入的AgNO3溶液,能与CO结合生成Ag2CO3白色沉淀,干扰Cl-的检验
3.如图所示是验证氯气性质的微型实验,a、b、c、d、e是浸有相关溶液的滤纸
向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面
已知:2KMnO4+16HCl(浓)===2KCl+5Cl2↑+2MnCl2+8H2O,下列选项正确的是()选项实验现象解释或结论Aa处变蓝,b处变红棕色氧化性:Cl2>Br2>I2Bc处先变红,后褪色氯气与水反应生成了酸性物质Cd处立即褪色氯气与水反应生成了漂白性物质De处变红色还原性:Fe2+>Cl-解析:选Da处变蓝,b处变红棕色只能说明氧化性:Cl2>Br2,Cl2>I2,A项错误;c处先变红,说明氯气与水反应生成了酸性物质,c处后褪色,是由于次氯酸具有漂白性,B项错误;d处Cl2与NaOH反应生成NaCl、NaClO和水,红色褪去可能是因为NaOH被消耗完造成,也有可能是生成漂白性物质,故不能说明一定是生成的物质具有漂白性,C项错误;e处变红色是因为Fe2+被氧化为Fe3+,Fe3+与SCN-反应生成红色溶液,由此可见还原性是Fe2+>Cl-,D项正确
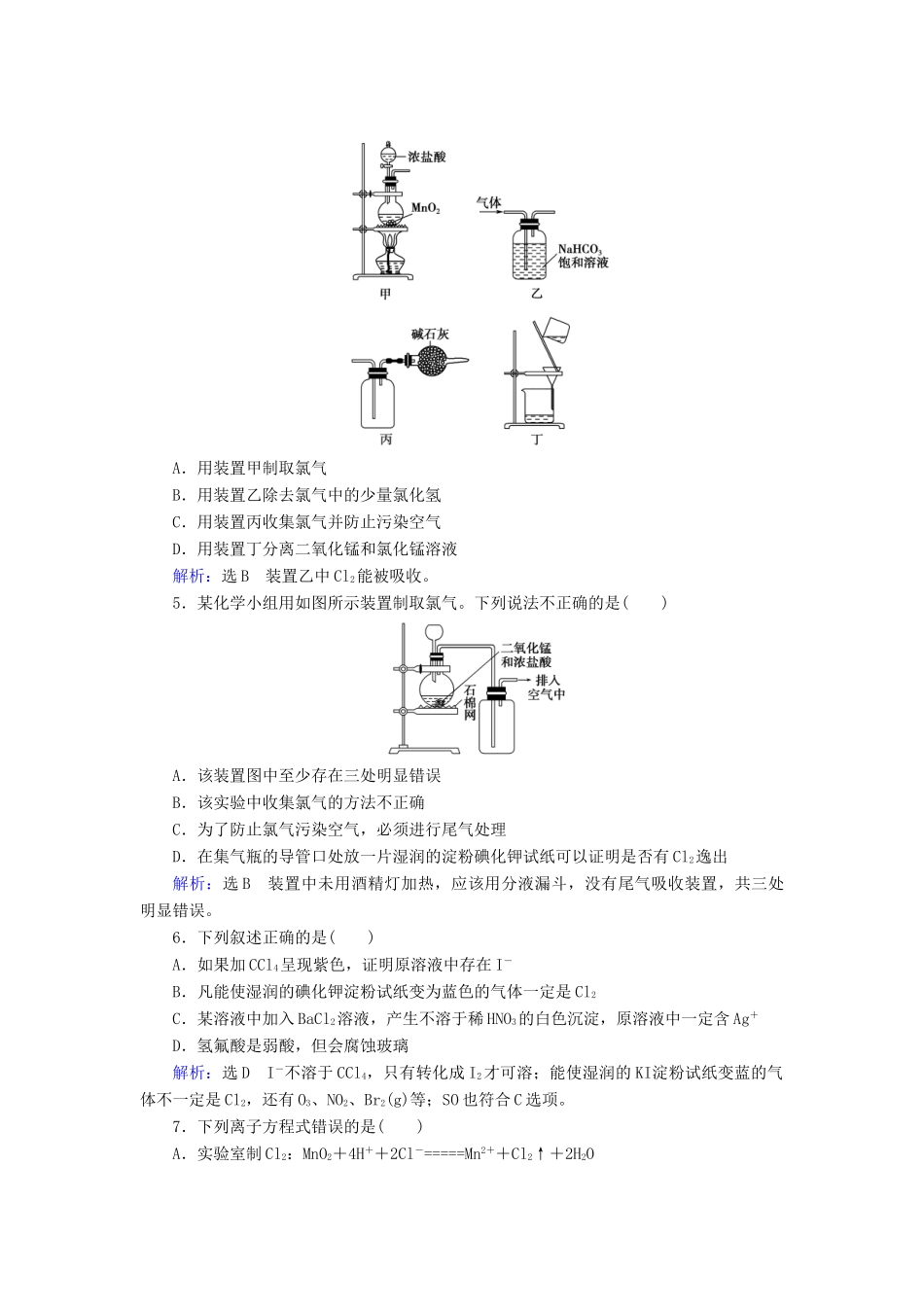
4.下列装置应用于实验室制取氯气并回收氯化锰溶液,不能达到实验目的的是()A.用装置甲制取氯气B.用装置乙除去氯气中的少量氯化氢C.用装置丙收集氯气并防止污染空气D.用装置丁分离二氧化锰和氯化锰溶液解析:选B装置乙中Cl2能被吸收