课后作业(二十一)[基础巩固]一、海水的综合利用1.海水是一个巨大的化学资源库,下列有关海水综合利用的说法错误的是()A.海水中含有溴元素,需经过化学变化才可以得到溴单质B.无论是海水波浪发电还是潮汐发电,都是将化学能转化为电能C.从海水中可以得到NaCl,电解熔融NaCl可制备金属钠D.从海水中提取镁可以采用下列方法:海水―→苦卤――→Mg(OH)2――→MgCl2溶液―→无水MgCl2―→MgCl2(熔融)――→Mg[解析]海水波浪发电是利用水面因波浪上下运动产生的能量来转化成电能;潮汐发电是利用潮涨和潮落形成的水的势能来转成电能;而将化学能转化为电能是原电池的反应原理
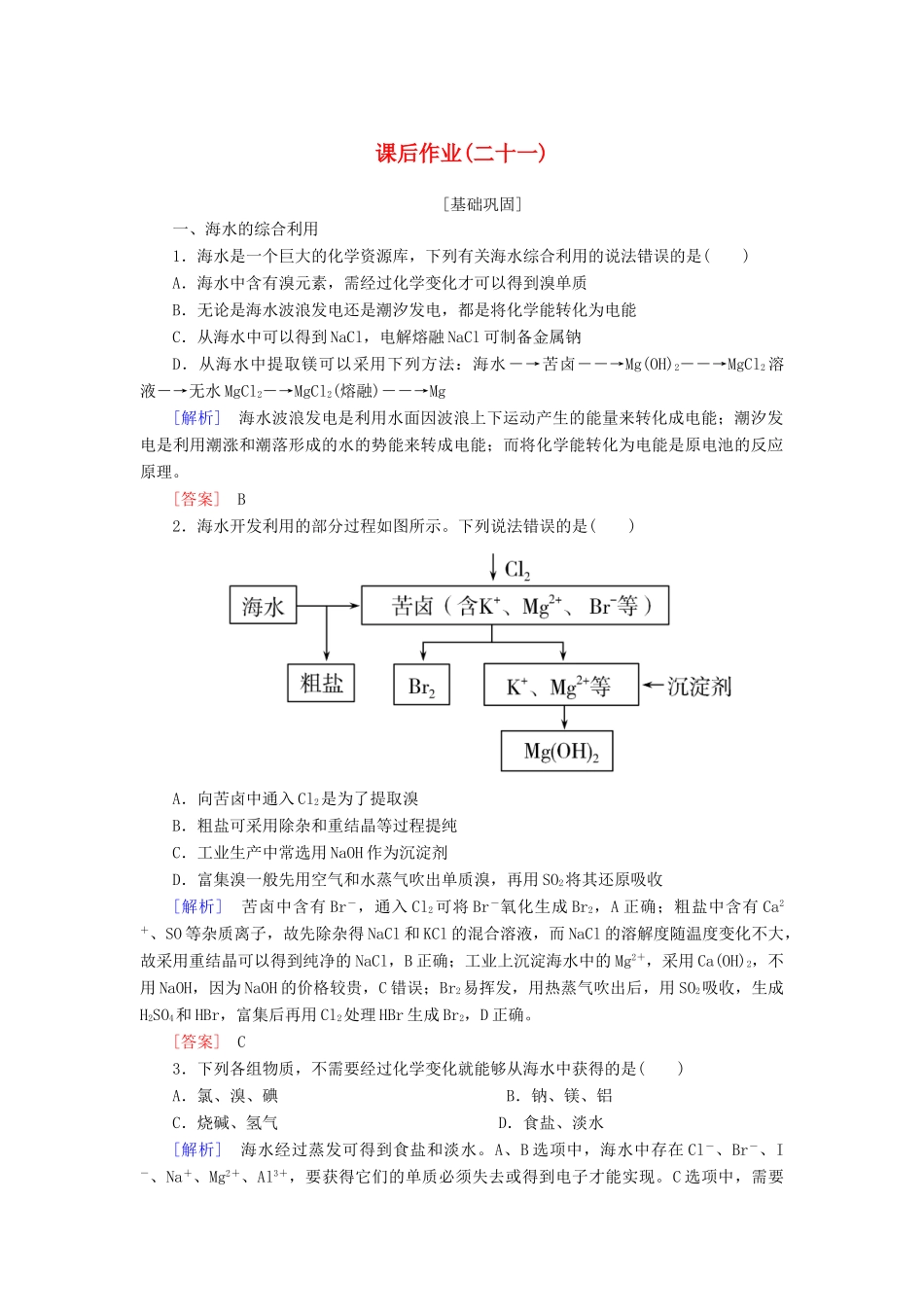
[答案]B2.海水开发利用的部分过程如图所示
下列说法错误的是()A.向苦卤中通入Cl2是为了提取溴B.粗盐可采用除杂和重结晶等过程提纯C.工业生产中常选用NaOH作为沉淀剂D.富集溴一般先用空气和水蒸气吹出单质溴,再用SO2将其还原吸收[解析]苦卤中含有Br-,通入Cl2可将Br-氧化生成Br2,A正确;粗盐中含有Ca2+、SO等杂质离子,故先除杂得NaCl和KCl的混合溶液,而NaCl的溶解度随温度变化不大,故采用重结晶可以得到纯净的NaCl,B正确;工业上沉淀海水中的Mg2+,采用Ca(OH)2,不用NaOH,因为NaOH的价格较贵,C错误;Br2易挥发,用热蒸气吹出后,用SO2吸收,生成H2SO4和HBr,富集后再用Cl2处理HBr生成Br2,D正确
[答案]C3.下列各组物质,不需要经过化学变化就能够从海水中获得的是()A.氯、溴、碘B.钠、镁、铝C.烧碱、氢气D.食盐、淡水[解析]海水经过蒸发可得到食盐和淡水
A、B选项中,海水中存在Cl-、Br-、I-、Na+、Mg2+、Al3+,要获得它们的单质必须失去或得到电子才能实现
C选项中,需要电解饱和食盐水获取
[答案]D4.海水总量极大,金、