第二节富集在海水中的元素——氯课后训练案巩固提升A组1
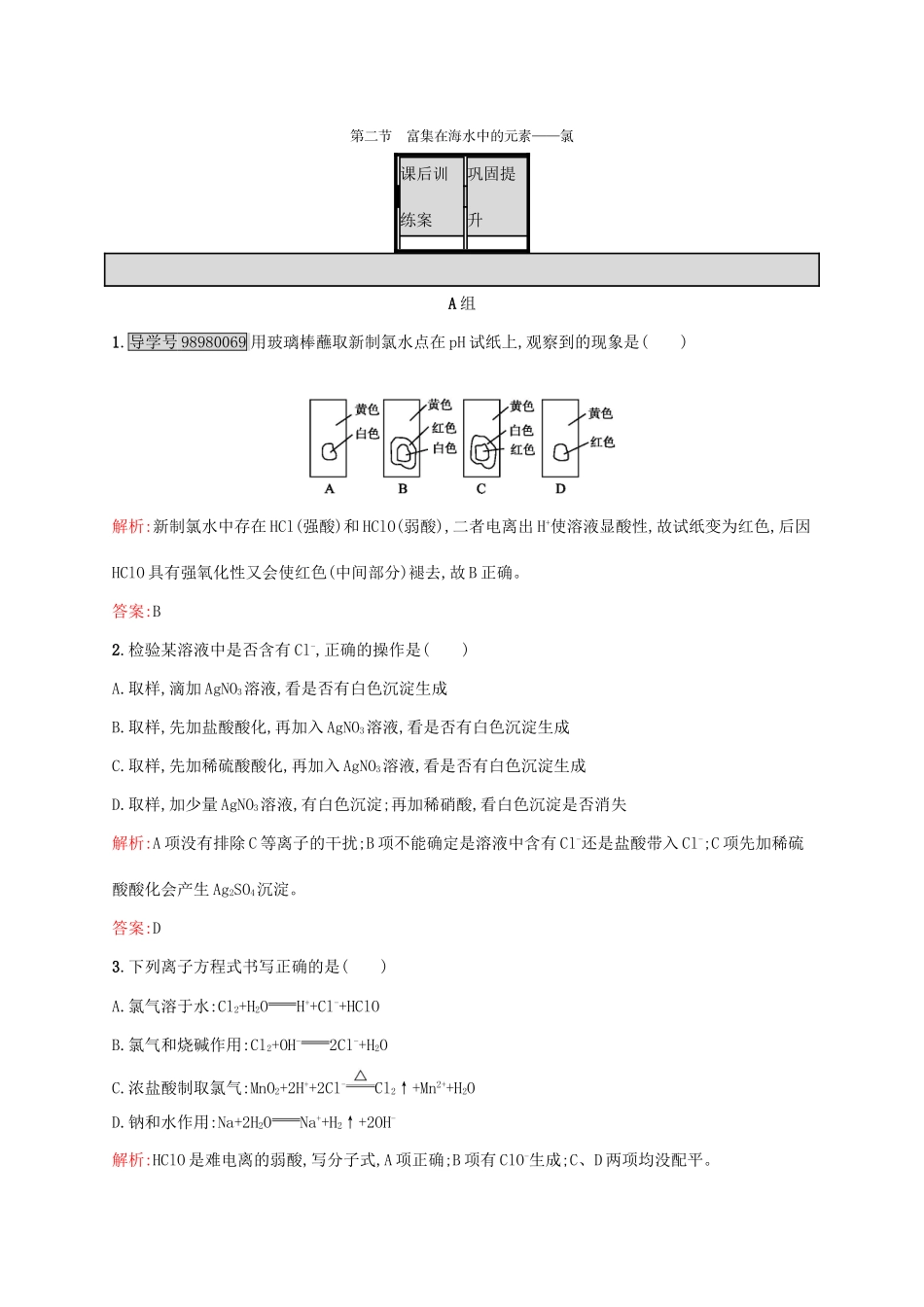
导学号98980069用玻璃棒蘸取新制氯水点在pH试纸上,观察到的现象是()解析:新制氯水中存在HCl(强酸)和HClO(弱酸),二者电离出H+使溶液显酸性,故试纸变为红色,后因HClO具有强氧化性又会使红色(中间部分)褪去,故B正确
检验某溶液中是否含有Cl-,正确的操作是()A
取样,滴加AgNO3溶液,看是否有白色沉淀生成B
取样,先加盐酸酸化,再加入AgNO3溶液,看是否有白色沉淀生成C
取样,先加稀硫酸酸化,再加入AgNO3溶液,看是否有白色沉淀生成D
取样,加少量AgNO3溶液,有白色沉淀;再加稀硝酸,看白色沉淀是否消失解析:A项没有排除C等离子的干扰;B项不能确定是溶液中含有Cl-还是盐酸带入Cl-;C项先加稀硫酸酸化会产生Ag2SO4沉淀
下列离子方程式书写正确的是()A
氯气溶于水:Cl2+H2OH++Cl-+HClOB
氯气和烧碱作用:Cl2+OH-2Cl-+H2OC
浓盐酸制取氯气:MnO2+2H++2Cl-Cl2↑+Mn2++H2OD
钠和水作用:Na+2H2ONa++H2↑+2OH-解析:HClO是难电离的弱酸,写分子式,A项正确;B项有ClO-生成;C、D两项均没配平
向盛有氯气的集气瓶中,注入约五分之一体积的下列液体并轻轻振荡,观察到的现象记录如图所示,判断瓶中注入的液体是()A
AgNO3溶液B
NaOH溶液C
FeCl2溶液解析:A项,Cl2作用于AgNO3溶液会产生AgCl白色沉淀;B项,Cl2与NaOH溶液反应会产生NaCl和NaClO,溶液呈无色;C项,Cl2溶于水,所得氯水呈浅黄绿色;D项,Cl2氧化FeCl2生成FeCl3,溶液呈棕黄色
下列说法中,正确的是()A
液氯和氯水都含有氯离子B
氯气和液氯都能使干燥的有色布条褪