第1课时金属矿物的开发利用学习目标核心素养建构1
了解金属在自然界中的存在形式
2.掌握金属的冶炼方法
3.掌握铝热反应原理及实验
4.了解金属回收和资源保护的意义,认识和体会化学在自然资源开发和利用中的意义和作用
[知识梳理]一、金属的冶炼1.金属在自然界中存在的形态除了金、铂等极少数金属以外,绝大多数金属以化合物的形式存在于自然界中
在这些金属化合物中,金属元素都显正化合价
2.金属冶炼的原理金属冶炼的实质是根据氧化还原反应,使金属矿物中的金属阳离子得到电子生成金属单质的过程:Mn++ne-===M
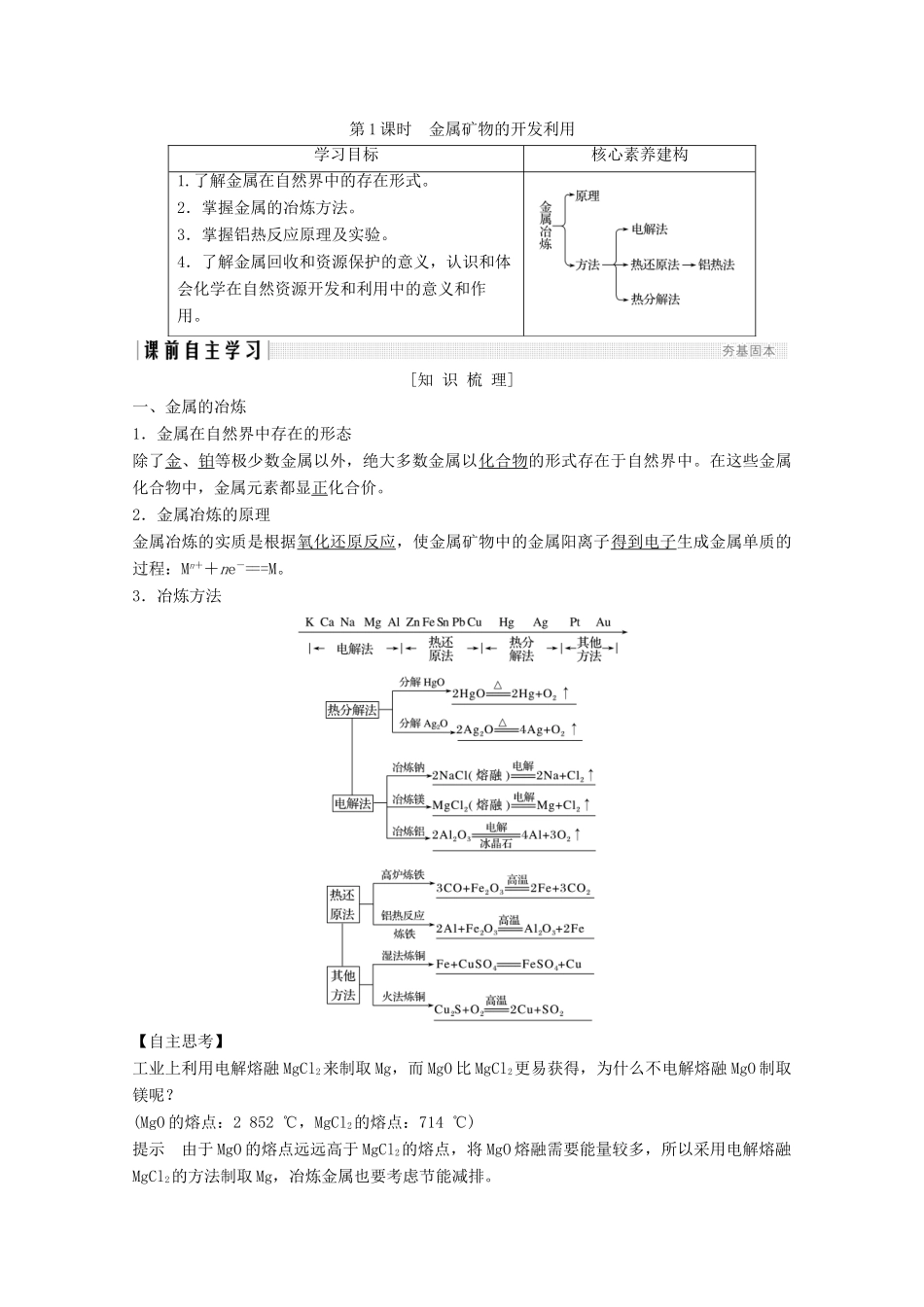
3.冶炼方法【自主思考】工业上利用电解熔融MgCl2来制取Mg,而MgO比MgCl2更易获得,为什么不电解熔融MgO制取镁呢
(MgO的熔点:2852℃,MgCl2的熔点:714℃)提示由于MgO的熔点远远高于MgCl2的熔点,将MgO熔融需要能量较多,所以采用电解熔融MgCl2的方法制取Mg,冶炼金属也要考虑节能减排
二、金属矿物的开发利用1.合理开发利用金属资源金属的冶炼需要消耗大量的资源和能源,还会造成环境污染,地球上的金属资源是有限的,是不可再生的,因此金属资源应合理地开发利用
2.有效利用金属资源的途径(1)提高金属的利用率,减少金属的使用量
(2)加强金属资源的回收和再利用
(3)使用其他材料代替金属材料
[效果自测]1.判断正误,正确的打“√”,错误的打“×”
(1)黄金的冶炼可用热分解法()(2)金属阳离子被还原,一定会得到金属单质()(3)工业上电解MgCl2溶液制取Mg()答案(1)×(2)×(3)×2.下列有关金属的工业制法中,正确的是()A.制钠:用海水为原料制得精盐,再电解纯净的NaCl溶液B.制铁:以铁矿石为原料,CO还原得铁C.制镁:用海水为原料,经一系列过程制得氧化镁固体,H2还原得镁D.制铝:从铝土矿中获得氧化铝再得到氯化铝固体,电解熔融的