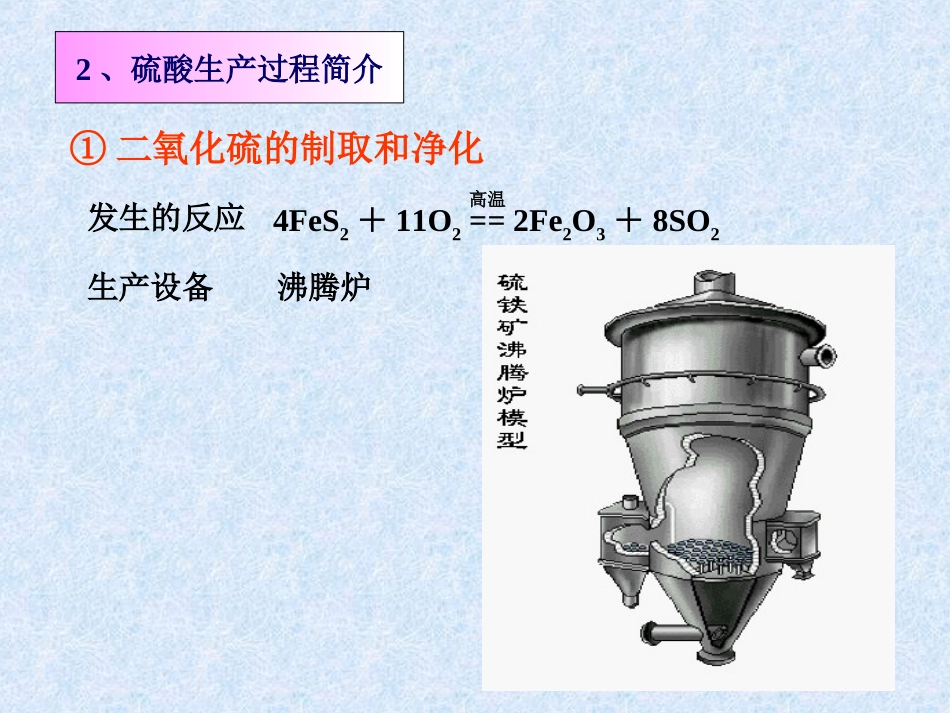
硫酸的工业制法思考:怎样制取硫酸?H2SO4SO3SO2SFeS2H2OO2O2O2①二氧化硫气体的制备S+O2SO2点燃4FeS2+11O22Fe2O3+8SO2高温②二氧化硫的催化氧化催化剂③三氧化硫的吸收SO3+H2O→H2SO41、接触法制硫酸的主要反应过程一、硫酸的工业制法-----接触法2SO2+O22SO3①二氧化硫的制取和净化发生的反应生产设备沸腾炉2、硫酸生产过程简介4FeS2+11O2==2Fe2O3+8SO2高温黄铁矿空气矿渣SO2、O2、N2沸腾炉炉气原料粉碎空气除尘洗涤干燥•为什么要将黄铁矿粉碎成细小矿粒?•为什么要从炉底通入强大空气流?讨论炉气的净化炉气的成分:净化的目的:方法:除尘(除矿尘)洗涤(除去砷、硒等化合物)干燥(除水蒸气)二氧化硫、氧气、氮气、水蒸气、矿尘、砷硒化合物等防止催化剂中毒和设备腐蚀②二氧化硫氧化成三氧化硫生产设备:接触室得到的气体:三氧化硫、氮气、未反应的氧气和二氧化硫发生的反应:2SO2+O22SO3V2O5经净化的SO2、O2SO2、O2SO3冷气体热气体温度较低的气体温度较高的气体接触室③三氧化硫跟水化合生成硫酸发生的反应:SO3+H2O==H2SO4用98.3%浓硫酸吸收三氧化硫生产设备:吸收塔98.3%H2SO4吸收塔尾气发烟H2SO4SO3O2、SO2、N22NH3+H2O+SO2=(NH4)2SO3(NH4)2SO3+H2SO4=(NH4)2SO4+H2O+SO2↑3、回收、净化处理尾气,保护环境。用氨吸收法回收二氧化硫化肥回收利用实验室用什么试剂吸收SO2?工业上是否适用?二、接触法制硫酸小结三阶段三方程三设备【例】含二氧化硅的黄铁矿样品10g在空气中充分燃烧,最后剩余8g残渣(残渣中不含硫元素)。又知在接触法制硫酸的生产中,有2%的硫受损失混入炉渣。用上述黄铁矿150t,可制得98%的浓硫酸多少吨?解:设10g黄铁矿中FeS2的质量为x4FeS2+11O2=2Fe2O3+8SO24×120g2×160gx10g–8g=2gx=6g黄铁矿中FeS2%=6÷10×100%=60%固体减重480g-320g=160g设150t含FeS260%的硫铁矿可制得98%的浓硫酸的质量为yFeS22H2SO4~120196150×60%×98%98%yy=147t答:可制得98%的浓硫酸147吨