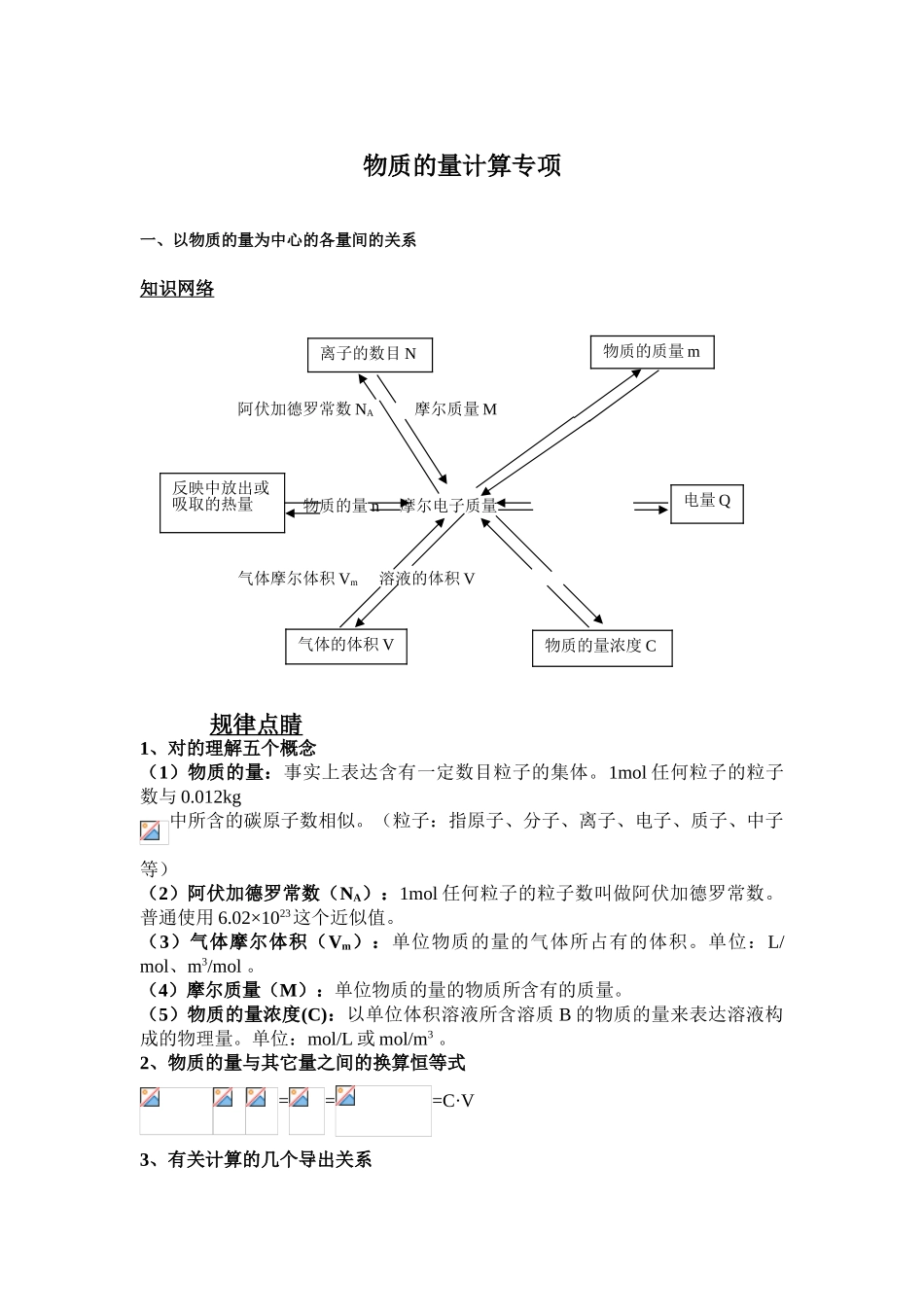
物质的量计算专项一、以物质的量为中心的各量间的关系知识网络阿伏加德罗常数NA摩尔质量M反映热物质的量n摩尔电子质量气体摩尔体积Vm溶液的体积V规律点睛1、对的理解五个概念(1)物质的量:事实上表达含有一定数目粒子的集体。1mol任何粒子的粒子数与0.012kg中所含的碳原子数相似。(粒子:指原子、分子、离子、电子、质子、中子等)(2)阿伏加德罗常数(NA):1mol任何粒子的粒子数叫做阿伏加德罗常数。普通使用6.02×1023这个近似值。(3)气体摩尔体积(Vm):单位物质的量的气体所占有的体积。单位:L/mol、m3/mol。(4)摩尔质量(M):单位物质的量的物质所含有的质量。(5)物质的量浓度(C):以单位体积溶液所含溶质B的物质的量来表达溶液构成的物理量。单位:mol/L或mol/m3。2、物质的量与其它量之间的换算恒等式===C·V3、有关计算的几个导出关系离子的数目N物质的质量m反映中放出或吸取的热量电量Q气体的体积V物质的量浓度C(1)求气态物质的摩尔质量或相对分子质量:M(g/mol)=ρg/L×22.4L/mol=A对B的相对密度×B的摩尔质量=mRT/PV(2)比较气体分子数目的多少:核心是比较气体的物质的量的大小。即:n1:n2=N1:N2(3)比较气体在相似条件下体积的大小:核心是比较气体的物质的量的大小。即:n1:n2=V1:V2(4)有关物质的量浓度的计算①C(B)=②C(浓溶液)·V(浓溶液)=C(稀溶液)·V(稀溶液)二、阿伏加德罗定律的应用知识网络概念:在相似的温度和压强下,相似体积的任何气体都含有相似数目的分子。同温、同压:n1:n2=V1:V2=N1:N2阿伏加德定律推论同温、同压、同质量:V1:V2=M1:M2同温、同压:ρ1:ρ2=M1:M2同温、同体积:n1:n2=p1:p2规律点睛1、气体的密度和相对密度原则状况下,气体的密度ρ(g/L)=M(g/mol)/22.4(L/mol)D(相对密度)=ρ1/ρ2=M1/M22、求相对分子质量M(或平均相对分子质量)的几个办法(1)M=22.4ρ(2)=【a、b为物质的量M(A)、M(B)为摩尔质量】(3)=M(A)·m%+M(B)·n%【m%、n%为A、B的体积分数】3、拟定气体分子构成若2体积气体Ax于1体积气体By正好完全反映生成A2B,由阿伏加德罗定律可知:气体的分子数之比等于体积比,即Ax:By:A2B=2:1:2,因此两气体反映物为双原子分子即A2和B2。4、气体反映中的计算同一气体反映中,各气体的体积比等于化学方程式中气体物质的化学计量数比。列式计算时,上下单位应一致,左右单位相对应。5、平均值规律及应用(1)根据:若M(A)>M(B),则M(A)>>M(B),代表平均相对原子质量、平均相对分子质量、平均浓度、平均含量、平均生成量、平均消耗量等。(2)应用:已知,能够拟定M(A)、M(B)的范畴;或已知M(A)、M(B),能够拟定的范畴。解题的核心是要通过平均值拟定范畴,诸多习题的平均值需要根据条件先拟定下来再作出判断。选择题1.设NA为阿伏加德罗常数,下列有关1L0.2mol/L的Ba(NO3)2溶液不对的的说法是()A.2L溶液中阴阳离子总数为0.8NA.B.500mL溶液中NO3-的浓度为0.4mol/L.C.500mL溶液中Ba2+的浓度为0.2mol/L.D.500mL溶液中NO3-的数目为0.2NA.2.实验室里需用480mL0.1mol/LCuSO4溶液,现选用500mL容量瓶进行配制,下列操作对的的是()A.称取7.68g硫酸铜,加入500mL水B.称取12.0g胆矾配成500mL溶液C.称取8.0g硫酸铜,加入500mL水D.称取12.5g胆矾配成500mL溶液3.VmLAl2(SO4)3溶液中含有Al3+ag,取溶液稀释到2VmL,则稀释后溶液中SO42-的物质的量浓度为()A.B.C.D.4.24mL浓度为0.05mol/L的Na2SO3溶液正好与20mL浓度为0.02mol/L的K2Cr2O7溶液完全反映,已知Na2SO3被K2Cr2O7氧化为Na2SO4,则元素Cr在还原产物中的化合价为()A.+2B.+3C.+4D.+55.氯气剧毒,化工厂惯用浓氨水检查管道与否泄漏氯气,反映化学方程式为:3Cl2+8NH3=6NH4Cl+N2当有10.65gCl2消耗时,被氧化的氨的质量为()A.3.4gB.1.7gC.6.8gD.0.85g6.将agNa2CO3和NaHCO3的混合物溶于水后配成1L溶液,经测定为0.5mol/L,若将ag原混合物加热至恒重的质量为()A.53.0gB.17.0gC.26.5gD.8.4g7.R2O8n-离子在一定条件下能够把Mn2+离子氧化为MnO4-离子,若反映后R2O8n-离子变成RO42-离子,又知反映中氧化剂与还原剂的物质的量之比为5:2,则R2O...