第二章化学反应与能量第二节化学能与电能(1)宁乡一中周志平学习目标:1、了解化学能与电能之间的相互转化关系2、初步认识原电池的概念、原理、组成条件、电极名称、电极反应和总反应及原电池的应用
3、通过反应物之间电子转移的探究,理解原电池的形成是氧化还原的本质的拓展和应用
重点:原电池的概念、原理、组成及应用难点:原电池的原理、组成条件、电极反应和总反应
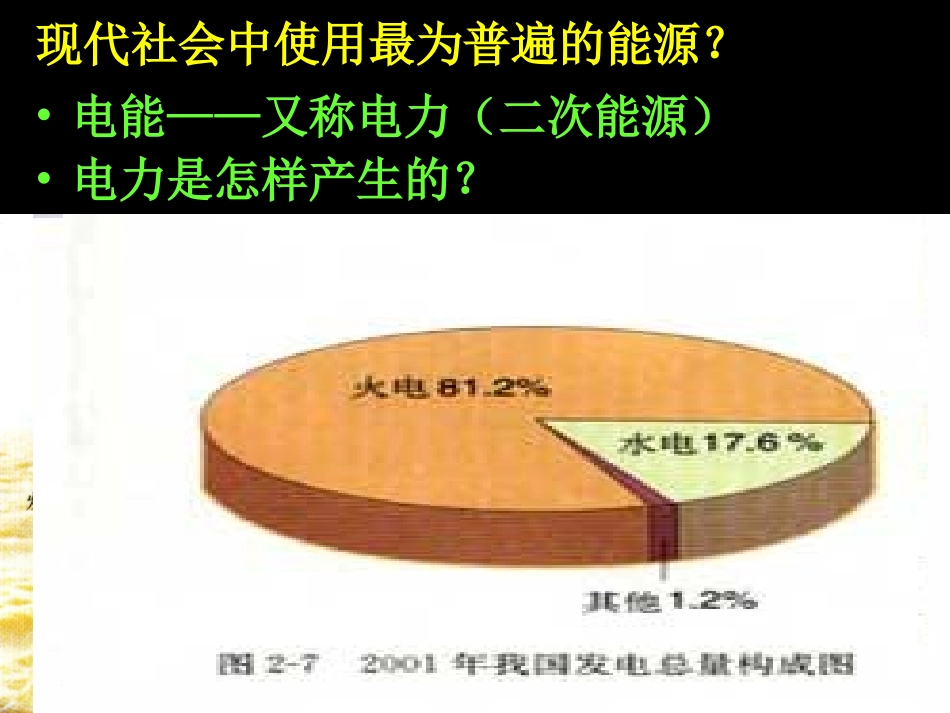
现代社会中使用最为普遍的能源
•电能——又称电力(二次能源)•电力是怎样产生的
一、化学能与电能的相互转化化学能(燃料)热能机械能电能燃烧蒸汽发电机(蒸汽轮机)(2)存在的问题:经多次转换,能量损耗大,燃料的利用率低;环境污染严重
(1)能量转换:1、火力发电(3)燃烧的本质是氧化还原反应,而氧化还原反应的本质是电子转移
2、原电池(1)定义:将化学能转变成电能的装置叫做原电池
较活泼金属较不活泼金属负极正极发生氧化反应发生还原反应e-I实验2-4(工作原理)现象:锌片不断溶解,铜片上有气泡产生,电流表的指针发生偏转
结论:电路中有电流通过,化学能转变成了电能
电子流出,电流流入电子流入,电流流出(2)电极名称:模拟动画(3)电极反应式负极:Zn–2e-=Zn2+氧化反应正极:2H++2e-=H2↑还原反应(4)总反应式(两个电极反应之和)Zn+2H+=Zn2++H2↑Zn+H2SO4(稀)=ZnSO4+H2↑原电池反应的本质是:氧化还原反应
(5)原电池原理:负极发生氧化反应,正极发生还原反应,电子从负极经外电路流向正极,从而产生电流,使化学能转变成电能
(电流方向呢
)(6)原电池组成条件①两种活泼性不同的金属(或其中一种为能导电的非金属,如“碳棒”)作电极其中较活泼金属为负极
较不活泼金属(或非金属)为正极(正极一般不参与电极反应,只起导电作用)
②电解质溶液(做原电池的内电路,并参与反应)③形成闭合回路④能自发地发生氧