十一单元十一单元盐化肥盐化肥l1
常见的盐有哪些,它们的用途是什么
盐的化学性质有哪些
碳酸根离子的检验方法
4常见的带颜色的盐有哪些
复分解反应的定义及发生的条件
粗盐的提纯步骤以及玻璃棒的作用
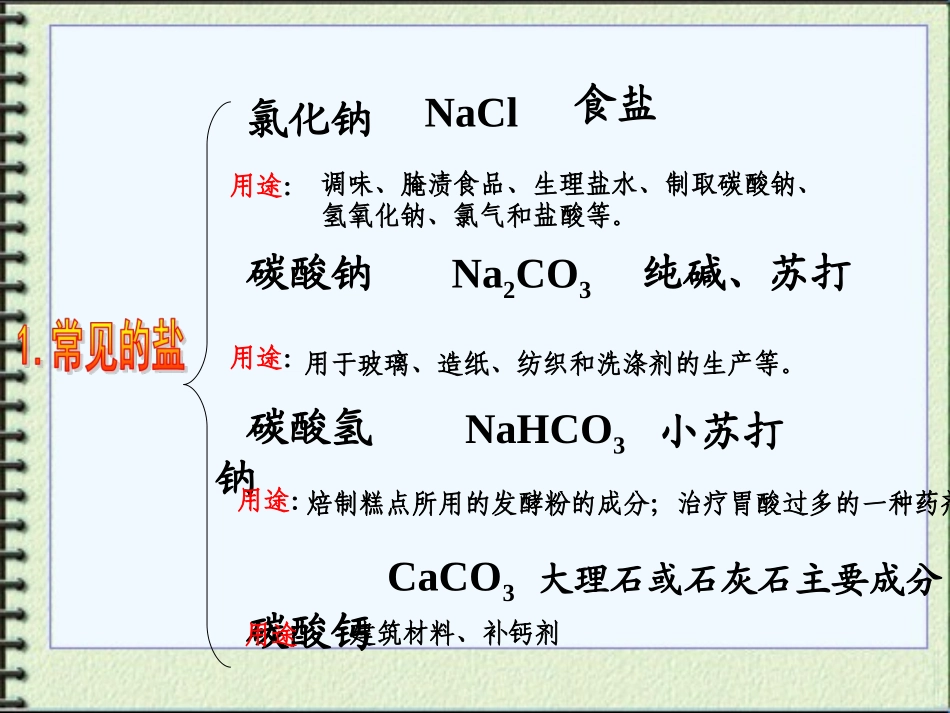
氯化钠碳酸钠碳酸氢钠碳酸钙NaCl食盐Na2CO3纯碱、苏打NaHCO3小苏打CaCO3大理石或石灰石主要成分用途:用途:用途:用途:调味、腌渍食品、生理盐水、制取碳酸钠、氢氧化钠、氯气和盐酸等
用于玻璃、造纸、纺织和洗涤剂的生产等
焙制糕点所用的发酵粉的成分;治疗胃酸过多的一种药剂建筑材料、补钙剂(1)(1)盐盐++金属——新盐金属——新盐++新金属新金属((置换反置换反应应))规律:应用:举例:反应物中盐要可溶,在金属活动性顺序中前面的金属将后面的金属从其盐溶液中置换出来(K、Ca、Na除外)判断或验证金属的活动性顺序和反应发生的先后顺序CuSO4+Fe=2AgNO3+Cu=3Cu(NO3)2+2Al=FeSO4+CuCu(NO3)2+2Ag2Al(NO3)3+3Cu二盐的化学性质(2)(2)盐盐++酸——新盐酸——新盐++新酸新酸((复分解反应复分解反应))•规律•应用•举例BaCl2+H2SO4=BaSO4↓+2HClCaCO3+2HCl=CaCl2+CO2↑+H2O反应物中的酸一般指硫酸、盐酸和硝酸
盐是碳酸盐时可不溶,若不是碳酸盐,则要求可溶
制取某些盐,制取二氧化碳气体等(3)(3)盐盐++碱——新盐碱——新盐++新新碱碱Na2CO3+Ca(OH)2=CaCO3↓+2NaOH•规律:反应物都可溶,生成物中沉淀生成;若反应物中盐为铵盐,则生成物中有气体
•举例:NH4Cl+NaOH=NaCl+NH3↑+H2OCuSO4+2KOH=K2SO4+Cu(OH)2↓制取某些碱MgCl2+Ca(OH)2=CaCl2+Mg(OH)2↓((复分解反应复分解反应))(