25/2/27第一节铝和铝的重要化合物导课实验探究小结练习25/2/27回忆金属的化学性质化学性质特点是均易最外层电子,表现性,且电子的能力越强,则金属性越强
主要表现:与非金属、酸、盐、氧化物等反应,在这些反应中,金属单质均作剂
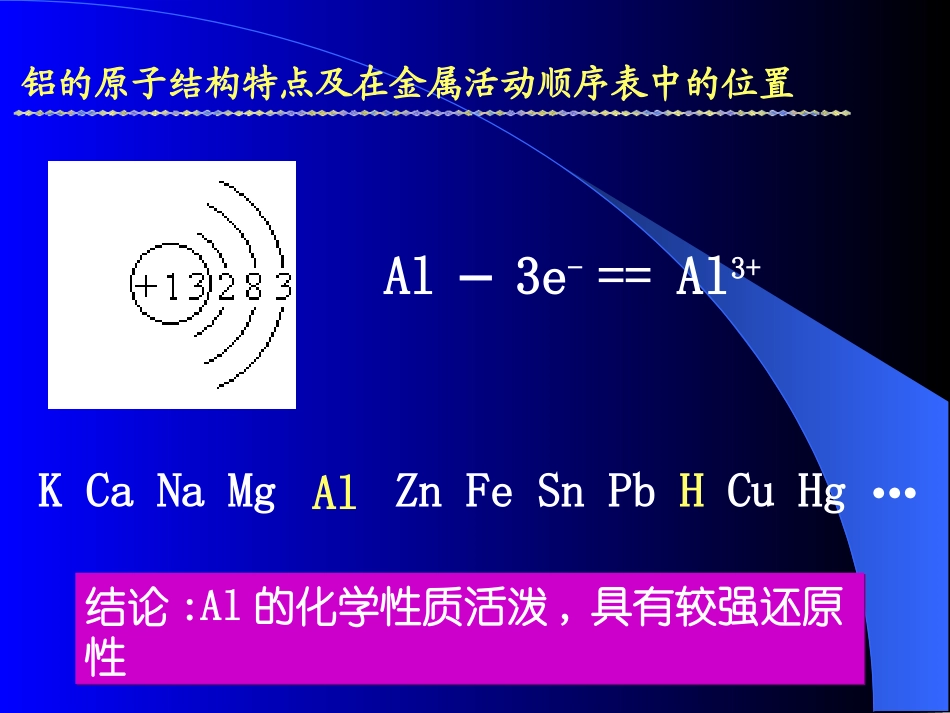
失去还原失去还原25/2/27铝的原子结构特点及在金属活动顺序表中的位置Al-3e-==Al3+KCaNaMgZnFeSnPbHCuHg…Al结论:Al的化学性质活泼,具有较强还原性结论:Al的化学性质活泼,具有较强还原性25/2/27①Al在氧气中燃烧②Al与酸反应③Al与NaOH溶液反应④Al与Fe2O3反应问题探究25/2/27演示【实验3-1】剧烈燃烧,放出大量的热和耀眼的白光现象:化学方程式:4Al+3O2==2Al2O3点燃25/2/27问题探究1
铝锅为什么可以用来煮饭
能写出Al和S、Cl2反应的化学方程式吗
2Al+3Cl2==2AlCl3点燃2Al+3S==Al2S3点燃常温下铝的表面被氧化,生成一层致密氧化物薄膜
因此铝具有抗腐蚀性
25/2/27演示【实验3-2】现象:镁与NaOH不反应,铝与NaOH反应,有氢气产生
化学方程式:2Al+2NaOH+2H2O==2NaAlO2+3H2↑25/2/27问题探究1
为什么铝制餐具不宜蒸煮或长期存放有酸性或碱性的食物
Al与氨水反应能生成H2吗
Al能与酸或碱起反应不能
Al与强碱反应才能生成H225/2/27演示【实验3-3】现象:化学方程式:发出耀眼的光芒,有熔融物生成2Al+Fe2O3==2Fe+Al2O3+Q高温铝热剂25/2/27问题探究1
铝热反应的原理
能写出下列方程式吗
Al把某些金属从它的氧化物中置换出来Al与V2O5Al与Cr2O325/2/27铝的用途结构→性质→用途1
制造导线和电缆;2
包装食品和饮料;制造日常用品;3
加入其他元素,制