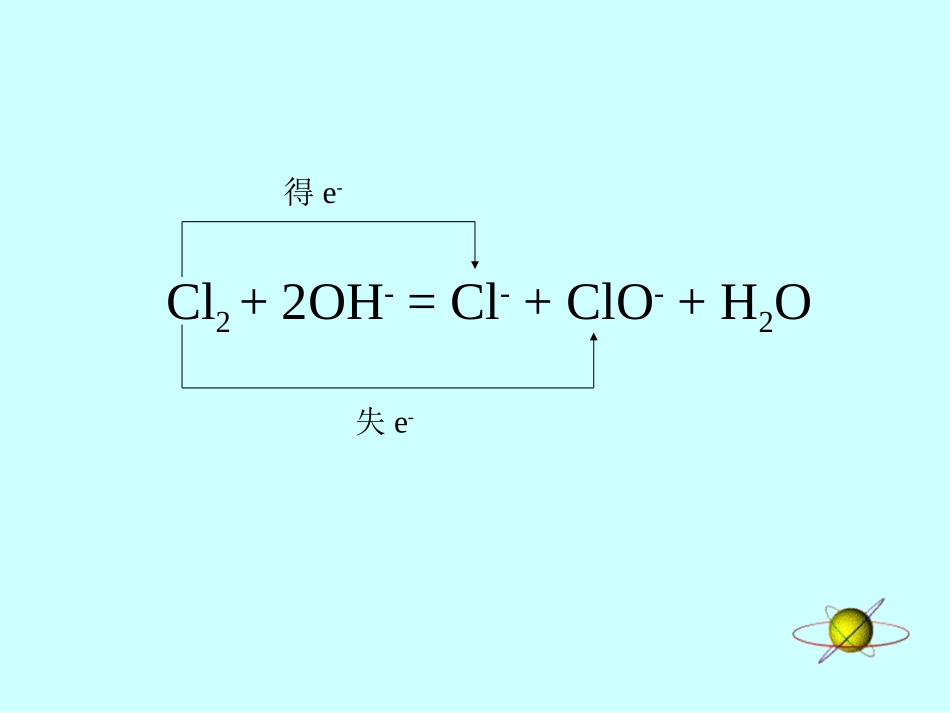
1、新制氯水和久置氯水有何区别2、写出Cl2与NaOH溶液反应的离子方程式,标明电子得失情况3、漂白粉是混合物还是纯净物其有效成分是什么成分:新制氯水(粒子):Cl2、H+、Cl-、HClO、H2O久置氯水(粒子):H+、Cl-新制氯水呈淡黄绿色,有漂白性久置氯水没有颜色,不具漂白性pH值:pH(新制氯水)>pH(久置氯水)表现:Cl2+2OH-=Cl-+ClO-+H2O得e-失e-漂白粉是CaCl2和Ca(ClO)2的混合物,其有效成分是Ca(ClO)2二、氯气的实验室制法1、原理:2、制取装置3、收集装置4、尾气吸收装置5、气体净化装置MnO2+4HCl(浓)==MnCl2+Cl2+2H2O1、用单双线桥标明电子得失情况2、所用的浓HCl是否全部被氧化,如果没有,被氧化的HCl和参加反应的HCl的物质的量之比是多少得2e-失2e-2e-1:2MnO2+4HCl(浓)==MnCl2+Cl2+2H2O△MnO2+4HCl(浓)==MnCl2+Cl2+2H2O△分析:反应物:固体+固体△气体固体+液体气体固体+液体气体△结论:烧瓶+分液漏斗液体+液体气体△分析:氯气的密度和溶解性1、氯气的密度大于相同状况下空气密度2、氯气能溶于水,但在饱和NaCl溶液中溶解度很小结论:1、向上排空气法2、不能用排水法,用排饱和食盐水法分析:氯气有毒,不能随便排入空气,应把它吸收用水吸收不完全,应用碱液来吸收,实验室中用NaOH溶液来吸收分析:1、能够吸收杂质气体2、不和所制备的气体反应所含杂质气体:HCl、H2O1、HCl用饱和食盐水吸收结论:2、H2O用浓H2SO4来吸收饱和NaCl溶液浓硫酸制备气体动画三、氯离子的检验[实验4-6]1、稀盐酸中滴入几滴AgNO3溶液2、NaCl溶液中滴入几滴AgNO3溶液3、Na2CO3中滴入几滴AgNO3溶液加入稀HNO3,现象如何
结论:Cl-的检验