第一章 卤 素 一、考纲要求1
掌握氯气、氯化氢的性质、用途和实验室制法,继而认识卤素的重要性质,用途和实验室制法
掌握漂白粉、氯化钠的生产和用途
掌握次氯酸的重要性质
掌握鉴别氯、溴、碘和卤化物的技能
会用化合价变化和电子转移的观点理解氧化、还原、氧化剂、还原剂等概念,并能判断氧化还原反应
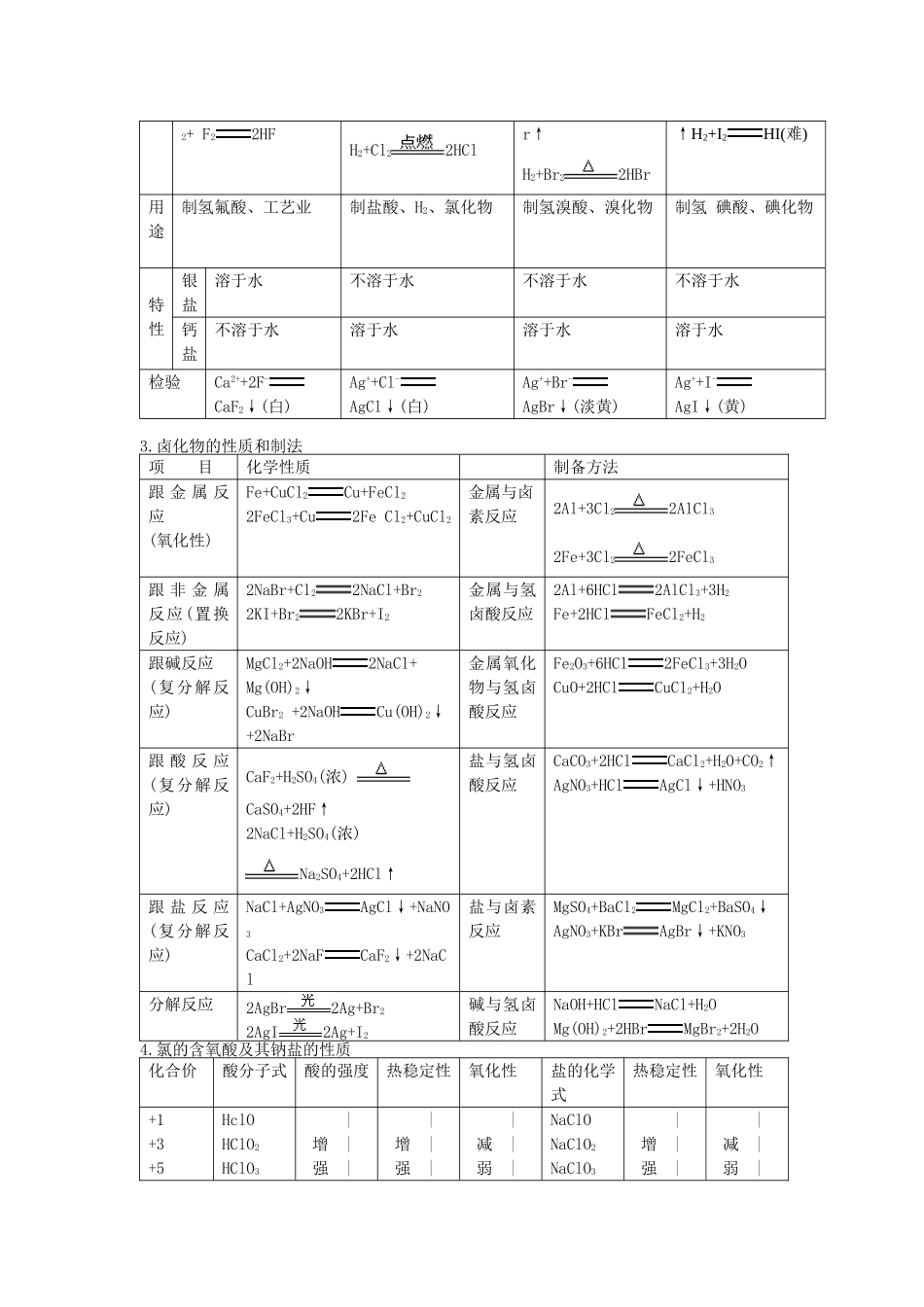
掌握卤化氢的性质、用途、制法,掌握溴化银和碘化银的性质和用途
掌握有一种反应物过量的化学方程式的计算
二、知识结构1
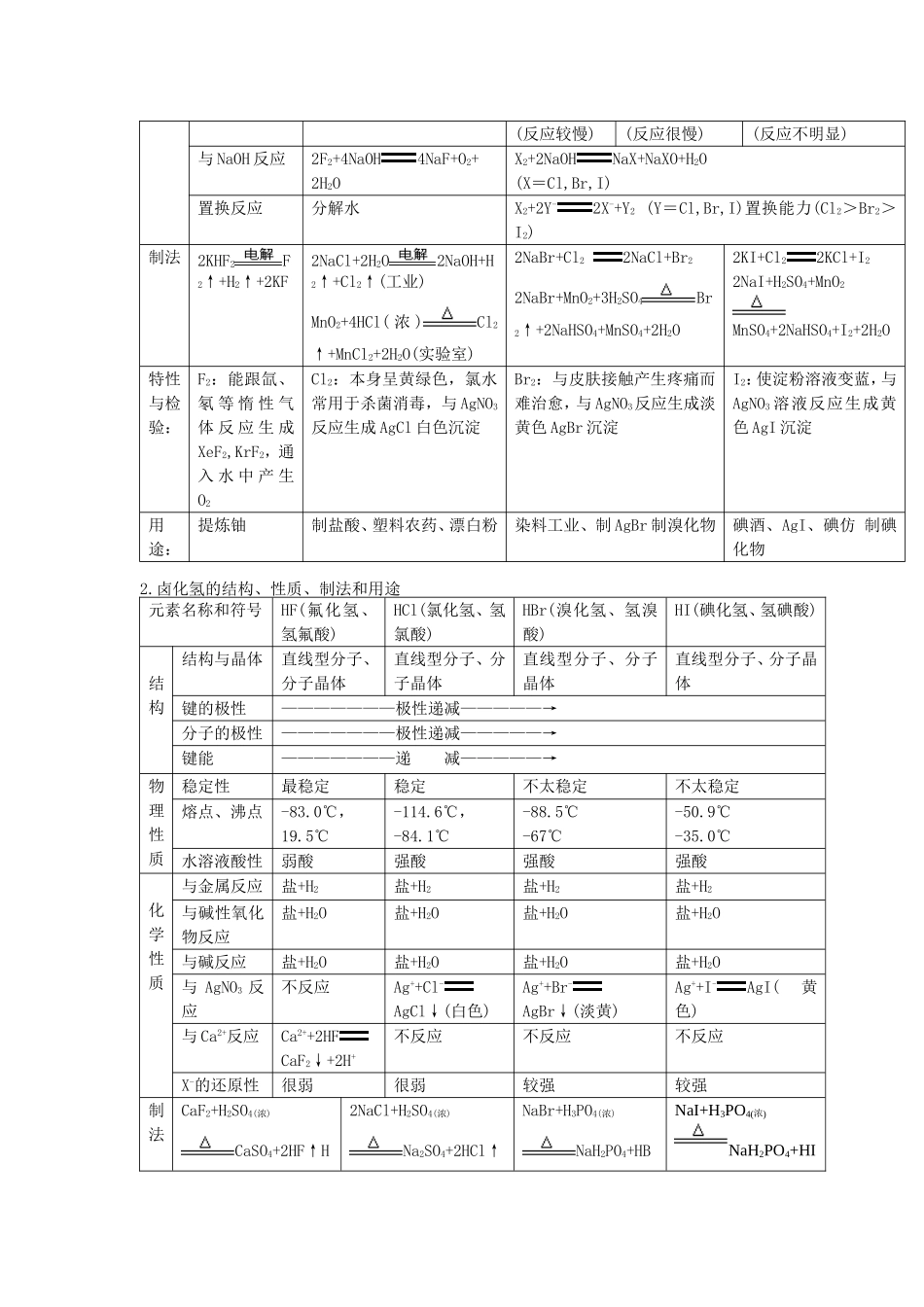
卤族元素原子结构、单质性质、制法和用途:元素名称和符号氟(F)氯(Cl)溴(Br)碘(I) 原子结构 原子序数9173553结构示意图电子式·F∶·C∶·rB∶· I∶主要化合价-1-1,+1,+3,+5,+7-1,+1,+3,+5-1,+1,+3,+5相同点最外层电子数相同,都是 7 个电子不同点原子核外电子层数不同,依次增大原子半径————————递增————————→阴离子半径————————递增————————→非 金 属 活 动性————————递增————————→原 子 氧 化 能力————————递增————————→阴 离 子 还 原能力————————递增————————→ 物理性质颜色和状态浅黄绿色气体黄绿色气体红棕色液体易挥发紫黑色固体易升华密度1
69 克/升3
214 克/升3
119 克 /厘米 34
93 克/厘米 3熔点(℃)————————递增————————→沸点(℃)————————递增————————→水中溶解性分解水————————递减————————→有机溶剂分解溶剂———————溶解性增大—————→ 化学反应`与金属反应nX2+2M2MXn 与大多数金属反应 反应快慢 F2>Cl2>Br2>I2与 H2反应X2+H22HX 反应剧烈程度 F2>Cl2>Br2>I