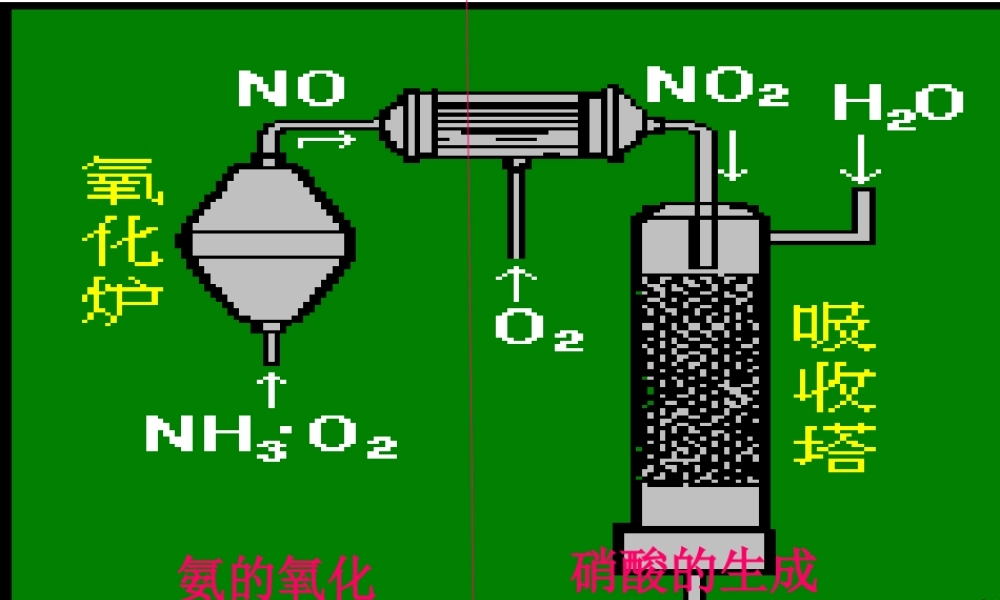
三、硝酸的制法 1 、实验室制法:NaNO3+H2SO4( 浓 )==NaHSO4+HNO3↑ △( 1 )原理:A 、 N2→NO→NO2→HNO3B 、 NH3→NO→NO2→HNO3C 、 NaNO3+HCl→HNO3D 、 NaNO3+H2SO4→HNO3( 2 )装置:曲颈瓶冰水 2 、工业制法: A 、 NaNO3+H2SO4→HNO3( 硝石法 )B 、 N2→NO→NO2→HNO3( 电弧法 ) C 、 NH3→NO→NO2→HNO3( 氨氧化 )氨的氧化硝酸的生成 氨的氧化硝酸的生成曲颈瓶( 2 )主要设备 氧化炉吸收塔( 3 )尾气 : NO 、 NO2 、 N2 等处理: 2NaOH+NO+NO2=NaNO3+H2O氨的氧化硝酸的生成1 、增大反应物的浓度2 、选择适当的温度3 、使用催化剂4 、增大反应物的接触面5 、反应物循环使用6 、利用化学反应放出的热 any.a4p