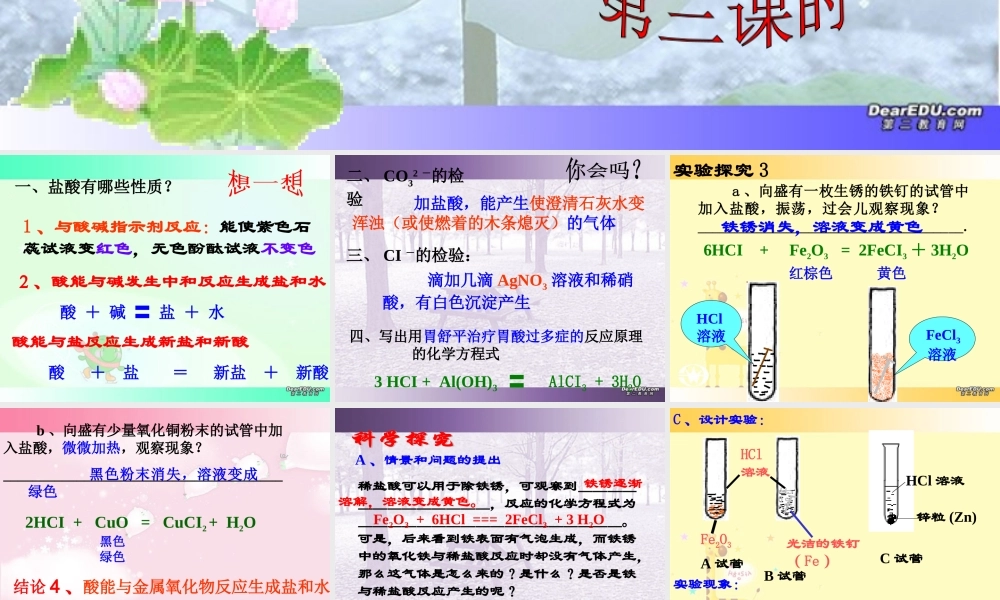
一、盐酸有哪些性质
1 、与酸碱指示剂反应:能使紫色石蕊试液变红色,无色酚酞试液不变色2、酸能与碱发生中和反应生成盐和水 酸 + 碱 〓 盐 + 水 3 、酸能与盐反应生成新盐和新酸 酸 + 盐 = 新盐 + 新酸二、 CO32 -的检验 加盐酸,能产生使澄清石灰水变浑浊(或使燃着的木条熄灭)的气体 滴加几滴 AgNO3 溶液和稀硝酸,有白色沉淀产生三、 CI -的检验:四、写出用胃舒平治疗胃酸过多症的反应原理 的化学方程式 3 HCI + Al(OH)3 〓AlCI3 + 3H2OHCl溶液 FeCl3溶液实验探究 3 a 、向盛有一枚生锈的铁钉的试管中加入盐酸,振荡,过会儿观察现象
____________________________________
铁锈消失,溶液变成黄色 6HCI + Fe2O3 = 2FeCI3 + 3H2O红棕色 黄色 b 、向盛有少量氧化铜粉末的试管中加入盐酸,微微加热,观察现象
______________________________________ 黑色粉末消失,溶液变成绿色2HCI + CuO = CuCI2 + H2O黑色 绿色结论 4 、酸能与金属氧化物反应生成盐和水 盐酸 +金属氧化物= 盐 + 水A 、情景和问题的提出稀盐酸可以用于除铁锈,可观察到_____________,反应的化学方程式为__________________
可是,后来看到铁表面有气泡生成,而铁锈中的氧化铁与稀盐酸反应时却没有气体产生,那么这气体是怎么来的
是否是铁与稀盐酸反应产生的呢
铁锈逐渐溶解,溶液变成黄色
Fe2O3 + 6HCl === 2FeCl3 + 3 H2O B 、你的假设是:铁等金属能与酸反应产生气体
C 、设计实验:Fe2O3HCl溶液光洁的铁钉( Fe )HCl 溶液锌粒 (Zn)实验现象:A 试管B 试管C 试管A