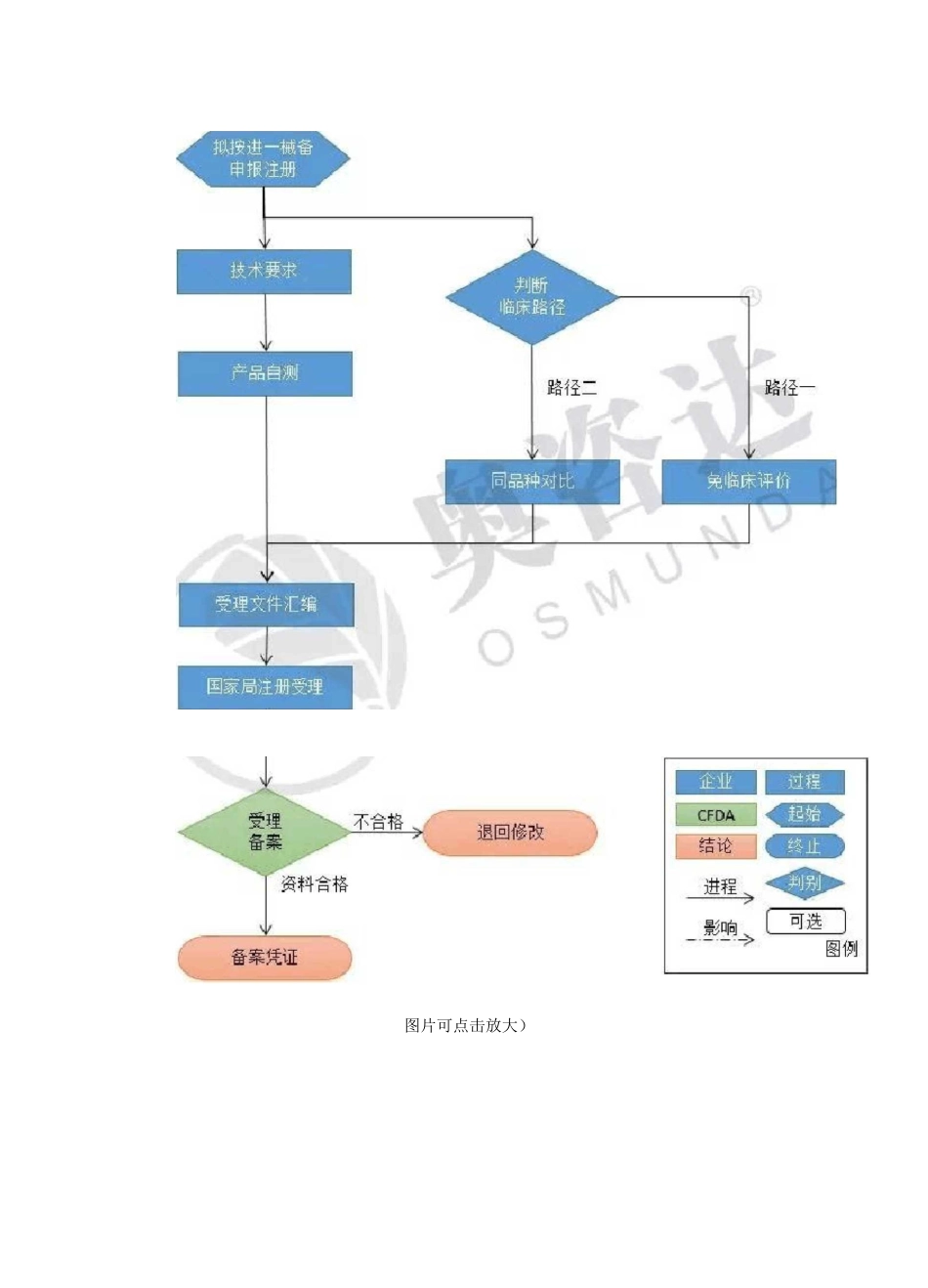
进口一类医疗器械备案流程医疗器械注册要求根据《医疗器械监督管理条例》(国务院令第 650 号)的规定,对医疗器械按照风险程度实行分类管理
第 I 类是风险程度低,实行常规管理可以保证其安全、有效的医疗器械,境内生产企业需要在所在地市药监局进行备案,境外医疗器械生产企业需要委托境内代理人在 CFDA 进行备案
第□类是具有中度风险,需要严格控制管理以保证其安全、有效的医疗器械,境内生产企业需要在所在地省(直辖市)药监局进行注册,境外医疗器械生产企业需要委托境内代理人在 CFDA 进行注册
第皿类是具有较高风险,需要采取特别措施严格控制管理以保证其安全、有效的医疗器械,无论境内、境外医疗器械生产企业均需要在 CFDA 进行注册
进口一类医疗器牺畜索流程图片可点击放大)L官方收费M 飙•《医疗器械监督管理条例》(国务院令第 650 号)•《医疗器械注册管理办法》(局令第 4 号)•《关于第一类医疗器械备案有关事项的公告》(第 26 号)•《关于发布第一类医疗器械产品目录的通告》(第 08 号)•《关于实施第一类医疗器械备案有关事项的通知》(食药监办械管[2014]174 号)时司分布当场受理详情可致电 400-6768632 咨询奥咨达
奥咨达服务项目CFDAII、III 类医疗器械注册咨询;CFDA 体外诊断试剂注册咨询;CFDA 进口 I、II、III 类医疗器械注册咨询;CFDAI 类医疗器械备案办理咨询;医疗器械优先审批办理咨询创新医疗器械审批申请服务欧盟 CE(MDD、IVDD、PPE、AIMDD);美国 FDA(列名、510K、PMA);全球注册(加拿大、澳大利亚、日本等)体系建立\内审\运行\考核服务;医疗器械临床试验服务;注册、体系、临床培训服务;高端医疗器械项目经验 Ik 心血管及血管外科I冠状动脉药物涂层球曩导管动脉导管未闭封堵器房间隔缺损封堵器药物球蠹扩张导