离 子 反 应 问题 1 :什么叫酸、碱、盐
电离时生成的阳离子全部是氢离子( H+ )的化合物叫做酸
电离时生成的阴离子全部是氢氧根离子 (OH-) 的化合物叫做碱
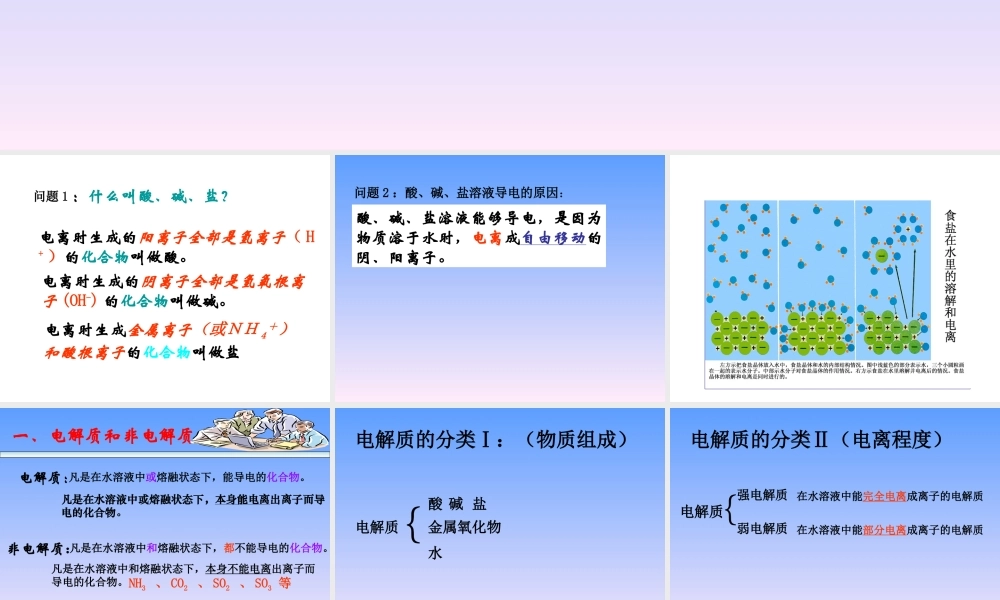
电离时生成金属离子(或NH4+)和酸根离子的化合物叫做盐 酸、碱、盐溶液能够导电,是因为物质溶于水时,电离成自由移动的阴、阳离子
问题 2 :酸、碱、盐溶液导电的原因: 一、电解质和非电解质电解质:凡是在水溶液中或熔融状态下,能导电的化合物
非电解质:凡是在水溶液中和熔融状态下,都不能导电的化合物
凡是在水溶液中或熔融状态下,本身能电离出离子而导电的化合物
凡是在水溶液中和熔融状态下,本身不能电离出离子而导电的化合物
一定要搞清本质
NH3 、 CO2 、 SO2 、 SO3 等 电解质的分类Ⅰ:(物质组成)电解质{酸 碱 盐金属氧化物水 电解质的分类Ⅱ(电离程度)电解质{强电解质弱电解质在水溶液中能完全电离成离子的电解质在水溶液中能部分电离成离子的电解质 强电解质的分类:强电解质{强酸 强碱 绝大多数盐金属氧化物( H2SO4 HCl HNO3 等)( NaOH KOH Ba(OH)2 等)( NaCl KNO3 BaSO4 CaCO3 等)( Na2O CaO 等) 弱电解质的分类:弱电解质{弱酸 弱碱 极少数盐水( H2CO3 H2S CH3COOH 等)( NH3
H2O Cu(OH)2 等) 强电解质弱电解质电离程度完全部分溶液里粒子水合离子分子、水合离子同条件下导电性强弱物质类别强碱、强酸、大多数盐弱碱、弱酸、水化合物类型离子化合物、某些共价化合物某些共价化合物强、弱电解质的比较 BaSO4 、 CaCO3 、 AgCl 等难溶于水的盐是否属电解质
CH3COOH 易 溶 , 是 否 属 强 电 解 质
想一想BaSO4 、 CaCO3 、 AgCl 虽然难溶,但溶解的极少部分却是完全