考点 11 Fe2%2b 与 Fe3%2b 的检验【考点定位】本考点考查 Fe2+与 Fe3+的常见检验方法,有明确两离子之间的相互干扰,特别是 Fe2+与 Fe3+的混合溶液中 Fe2+的检验方法及两离子的检验在物质推断与混合物成分鉴别中的应用
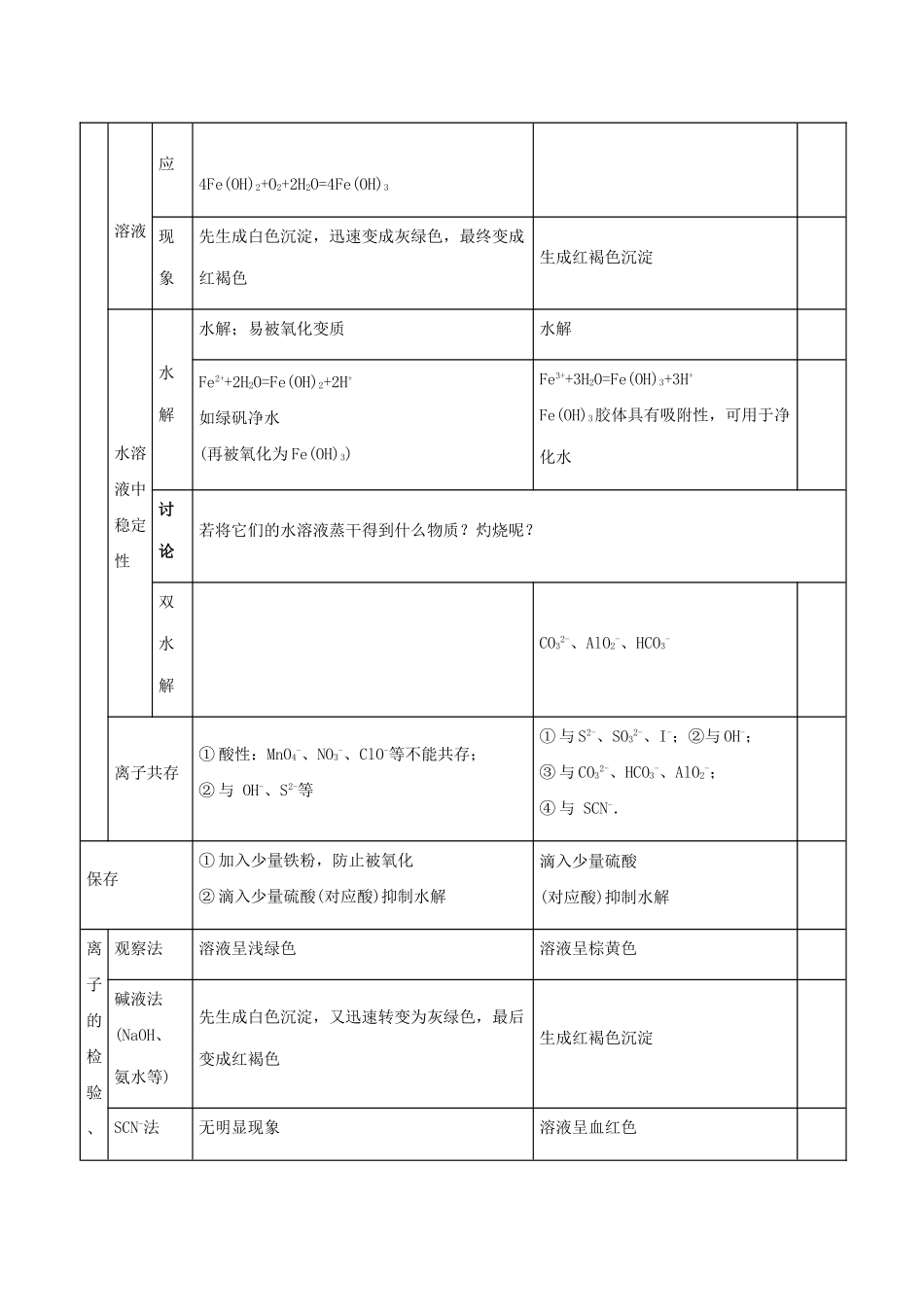
【精确解读】一、Fe2+、Fe3+的比较离子Fe2+[FeSO4]Fe3+[Fe2(SO4)3] 溶液中颜色浅绿色棕黄色 化学性质氧化剂HNO33Fe2++4H++NO3- =3Fe3++2H2O+NO↑不反应 O3、H2O2等将 Fe2+氧化成 Fe3+还原剂Na2SFe2++S2-=FeS↓2Fe3++S2-(少)=2Fe2++S↓2Fe3++3S2-(过)=2FeS↓+S↓ H2S不反应2Fe3++S2-(少.过)=2Fe2++S↓ 小结①FeS 能溶于硫酸、盐酸②CuS 不溶于稀硫酸、盐酸;但能溶于具有强氧化性的硝酸HI不反应2Fe3++2I-=2Fe2++I2不反应总结①Fe2+具有还原性,易被氧化;加入氧化剂,溶液由浅绿色变为棕黄色②Fe3+具有强氧化性,可以氧化还原性较强的物质③Cu2+相对稳定,不具有强氧化性,也不具有强还原性NaOH 反Fe2++2OH-=Fe(OH)2↓Fe3++3OH-=Fe(OH)3↓ 溶液应4Fe(OH)2+O2+2H2O=4Fe(OH)3现象先生成白色沉淀,迅速变成灰绿色,最终变成红褐色生成红褐色沉淀 水溶液中稳定性水解水解;易被氧化变质水解 Fe2++2H2O=Fe(OH)2+2H+如绿矾净水(再被氧化为 Fe(OH)3)Fe3++3H2O=Fe(OH)3+3H+Fe(OH)3胶体具有吸附性,可用于净化水 讨论若将它们的水溶液蒸干得到什么物质
双水解CO32-、AlO2-、HCO3- 离子共存① 酸性:MnO4-、NO3-、ClO-等不能共存;② 与 OH-、S2-等① 与 S