第 2 课时 铝的重要化合物课程目标1.掌握铝的重要化合物的主要性质及应用
2.了解铝的化合物相互转化的关系及图像
3.了解两性氧化物和两性氢氧化物的概念
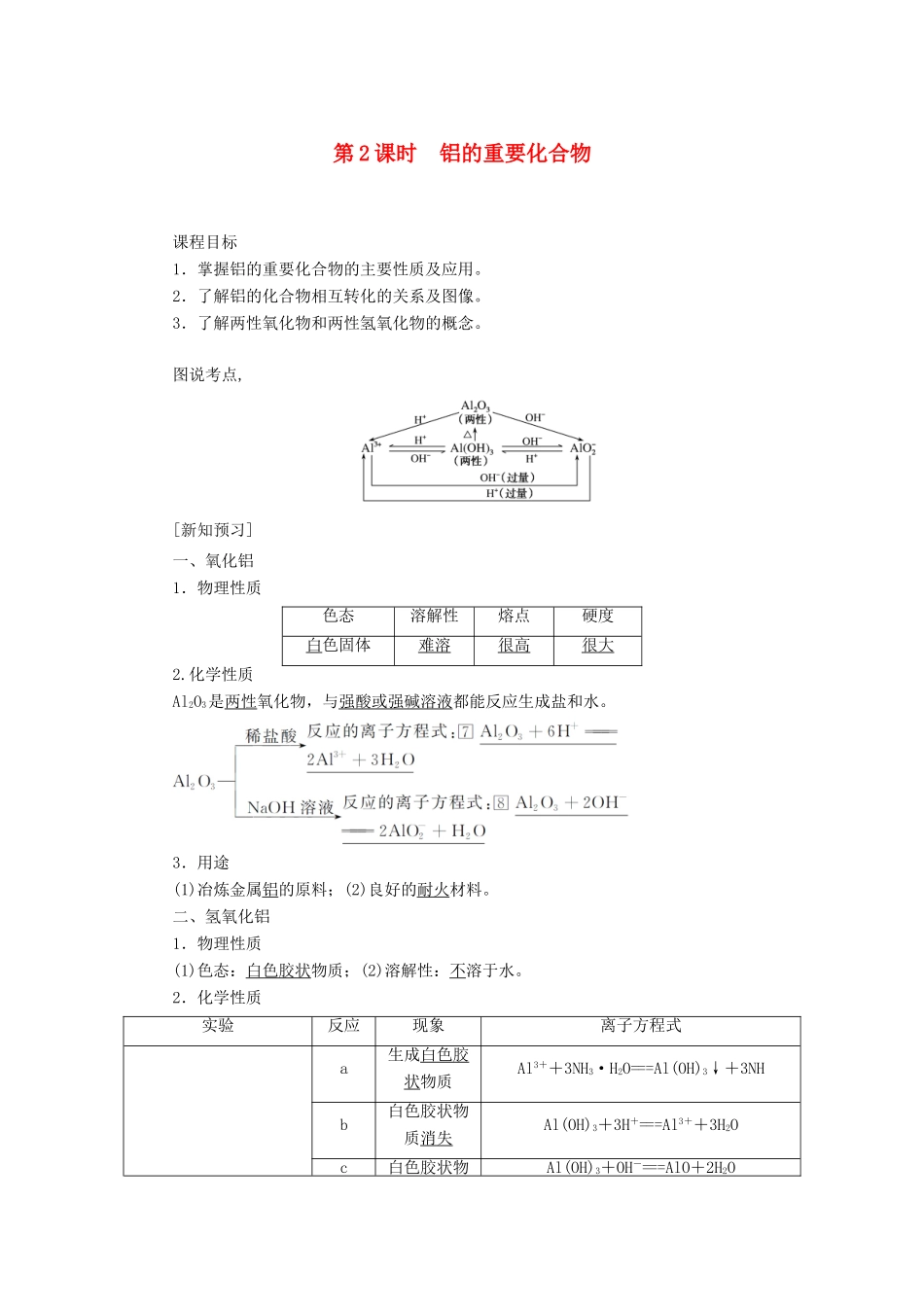
图说考点, [新知预习]一、氧化铝1.物理性质色态溶解性熔点硬度白色固体难溶很高很大2
化学性质Al2O3是两性氧化物,与强酸或强碱溶液都能反应生成盐和水
3.用途(1)冶炼金属铝的原料;(2)良好的耐火材料
二、氢氧化铝1.物理性质(1)色态:白色胶状物质;(2)溶解性:不溶于水
2.化学性质实验反应现象离子方程式a生成白色胶状物质Al3++3NH3·H2O===Al(OH)3↓+3NHb白色胶状物质消失Al(OH)3+3H+===Al3++3H2Oc白色胶状物Al(OH)3+OH-===AlO+2H2O质消失Al(OH)3是两性氢氧化物,难溶于水
Al(OH)3不稳定,受热分解为 Al2O3和 H2O,反应方程式为 2Al(OH)3=====Al2O3+3H2O
3.用途(1)能凝聚水中的悬浮物,并能吸附色素,可用来净水
(2)利用其弱碱性,可作胃酸中和剂
三、硫酸铝钾(1)电离方程式: KAl(SO4)2===K++Al3++2SO(2)十二水合硫酸铝钾的化学式为 KAl(SO4)2·12H2O,俗名明矾,是一种无色晶体,可溶于水,可用作净水剂
[即时性自测]1.判断正误,正确的打“√”,错误的打“×”(1)Al2O3熔点高,可用作耐高温材料
( )(2)把氯化铝溶液滴入浓氢氧化钠溶液中,产生大量白色沉淀
( )(3)制备 Al(OH)3悬浊液:向 1 mol·L-1AlCl3溶液中加过量的 6 mol·L-1NaOH 溶液
( )(4)氢氧化铝可作胃酸的中和剂
( )(5)明矾作净水剂,明矾起还原作用
( )答案:(1)√ (2)× (3)× (4)√ (5)×2.下列有关铝的化合物的叙述中,不正确的是( )A.