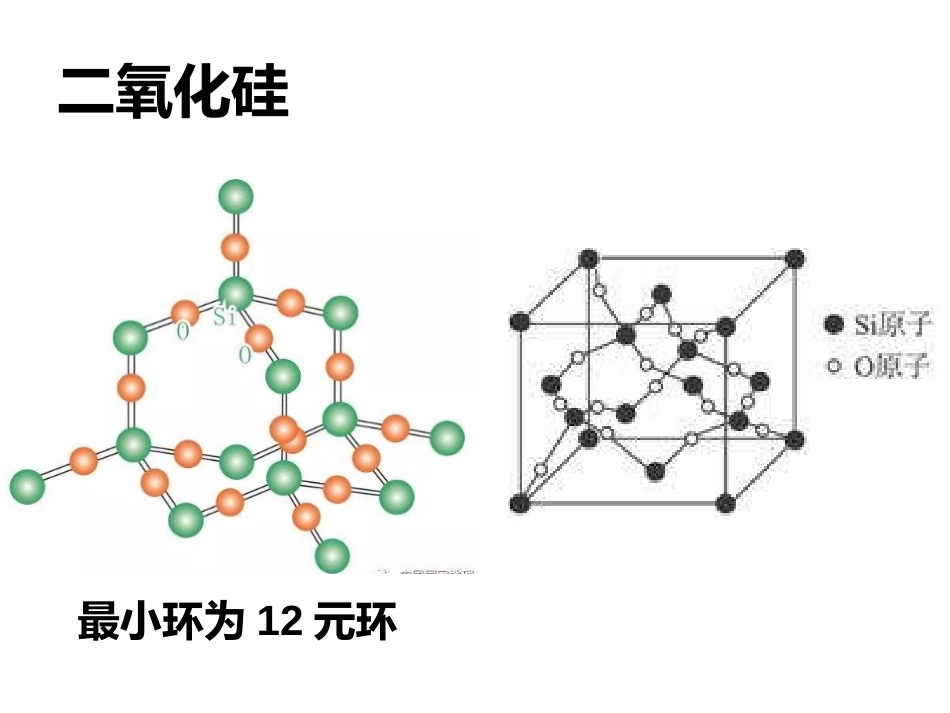
二轮复习晶体结构填充方式问题附升级练习原子晶体:金刚石每个C原子被个六元环所共用!12二氧化硅最小环为12元环分子晶体(范德华力vs氢键)•课本P65•如果分子间作用力只是范德华力,其周围通常可以有12个紧邻的分子。这一特征叫分子密堆积C60配位数为12冰晶体中水分子的配位数为4作用力越强,收缩的越紧,配位数越小这是什么晶体呢?离子晶体(离子键)•NaCl同号阴离子相切异号离子相切同号异号均相切你觉得那种情况会比较稳定呢?三次配位正负离子最小半径比的计算三次配位——平面三角形配位从图所示,根据平面几何得下式:2r-sin60º×2/3=r-+r+两端同除以r-,得:r+/r-=2sin60º×2/3-1=0.155所以,阳离子要形成三次配位结构,阳离子的最小半径应为阴离子半径的0.155倍以上。四次配位正负离子最小半径比的计算四次配位——四面体配位如图所示,我们可依四面体画一立方体,立方体的面对角线的长度为2r-,立方体的体对角线的长度为2(r-+r+)设立方体的边长为a,根据立体几何:√2×a=2r-;√3×a=2(r-+r+)即:√2r-=2√3r-/3+2√3r+/3两端同除以r-,得√2=2√3/3+2√3/3×r+/r-即r+/r-=(√2-2√3/2)/2√3/3=3√2/2√3-1=0.225所以,阳离子要形成四次配位结构,阳离子的最小半径应为阴离子半径的0.225倍以上。六次配位正负离子最小半径比的计算六次配位——八面体配位如图所示,根据平面几何得下式:2√2r-=2r-+2r+两端同除以r-,得:r+/r-=√2-1=0.414所以,阳离子要形成六次配位结构,阳离子的最小半径应为阴离子半径的0.414倍以上。八次配位正负离子最小半径比的计算八次配位——立方体配位从图所示,根据立体几何得下式:2√3r-=2r-+2r+两端同除以r-,得:r+/r-=√3-1=0.732所以,阳离子要形成八次配位结构,阳离子的最小半径应为阴离子半径的0.732倍以上。硒化锌的晶胞结构如图所示,该晶胞中硒原子所处的空隙类型为(填“立方体”“正八面体”或“正四面体”),该种空隙的填充率为。正四面体50%MgO具有NaCl型结构(如图),其中阴离子采用面心立方最密堆积方式,X射线衍射实验测得MgO的晶胞参数为a=0.420nm,则r(O2-)为nm。MnO也属于NaCl型结构,晶胞参数为a’=0.448nm,则r(Mn2+)为nm0.1480.076某铬的氧化物晶体结构如图甲所示,则该氧化物的化学式可表示为,氧原子为六方最密堆积,铬原子处于氧原子所构成的八面体间隙中,如果乙所示,图中氧原子所组成的八面体间隙被铬原子占据的与未占据的占空比为。Cr2O32:1已知FexO晶体晶胞结构为NaCl型,由于晶体缺陷,x值小于1.测知FexO晶体密度为5.71g/cm3,晶胞边长为4.28×10-10m,(铁的相对原子质量取55.9,氧的相对原子质量取16)。求①在晶体中,铁元素的离子间最短距离为多少?②晶体中Fe分别为+2价,+3价,求亚铁离子所占的百分数(用小数表示,精确至0.001)。③此晶体的化学式。0.826单质铁可以与氧形成多种氧化物Fe3O4晶体中,O2﹣的重复排列方式如图所示,该排列方式中存在着由如1、3、6、7的O2﹣围成的正四面体空隙和3、6、7、8、9、12的O2﹣围成的正八面体空隙。Fe3O4中有一半的Fe3+填充在正四面体空隙中,另一半Fe3+和Fe2+填充在正八面体空隙中,则Fe3O4晶体中,正四面体空隙数与O2﹣数之比为,有%的正八面体空隙没有填充阳离子。Fe3O4晶胞中有8个图示结构单元,晶体密度为5.18g/cm3,则该晶胞参数a=pm.(写出计算表达式)2:150正四面体空隙有8个,正八面体空隙有4个;假设共三个铁离子,一个三价铁填入四面体空隙剩下两个铁离子填入八面体空隙,所以八面体填充率为50%