1 原子结构 1、根据构造原理写出1~36 号元素原子的电子排布式 2、核外电子的运动状态,电子云与原子轨道,基态、激发态和光谱 3、泡利原理、洪特规则 一、原子结构模型的演变 1
1869 年,俄国化学家门捷列夫发现了元素周期表 2
19 世纪初,道尔顿提出了近代原子学说 3
1913 年,丹麦科学家玻尔提出了氢原子模型 4
1920 年,丹麦科学家波尔提出了构造原理 5
1925 年,丹麦科学家波尔的“壳层” 落实为“能层” 与“能级” 厘清了核外电子的可能状态 6
1936 年,德国科学家马德隆发表了以原子光谱事实为依据的完整的构造理论 二、能层与能级 1
能层(相当于必修中的电子层) (1)定义:核外电子按能量不同分成能层
(2)电子的能层由内向外排序,其序号、符号以及所能容纳的最多电子数及能层的能量与能层离原子核距离的关系: 能层 一 二 三 四 五 六 七 符号 K L M N O P Q 最多电子数 2 8 18 32 50 72 98 离核远近 近 远 能量高低 低 高 即能层越高,电子的能量越高,离原子核越远 (3)能层数量规律: ①每一层最多容纳的电子数:2n2 个
②最外层电子数不超过8 个(K 层为最外层时不超过2 个)
③次外层电子数不超过18 个,倒数第三层不超过32 个
(4)能层能量规律: ①原子核外电子总是尽可能先排布在能量较低的能层上,然后由内向外依次排布在能量逐渐升高的能层
②能层越高,电子的能量越高
③能量的高低顺序为E(K)<E(L)<E(M)<E(N)<E(O) 2 <E(P)<E(Q)
能级 (1)定义:同一能层的电子,还被分成不同能级
(2)表示方法:分别用相应能层的序数和字母s、p、d、f 等表示
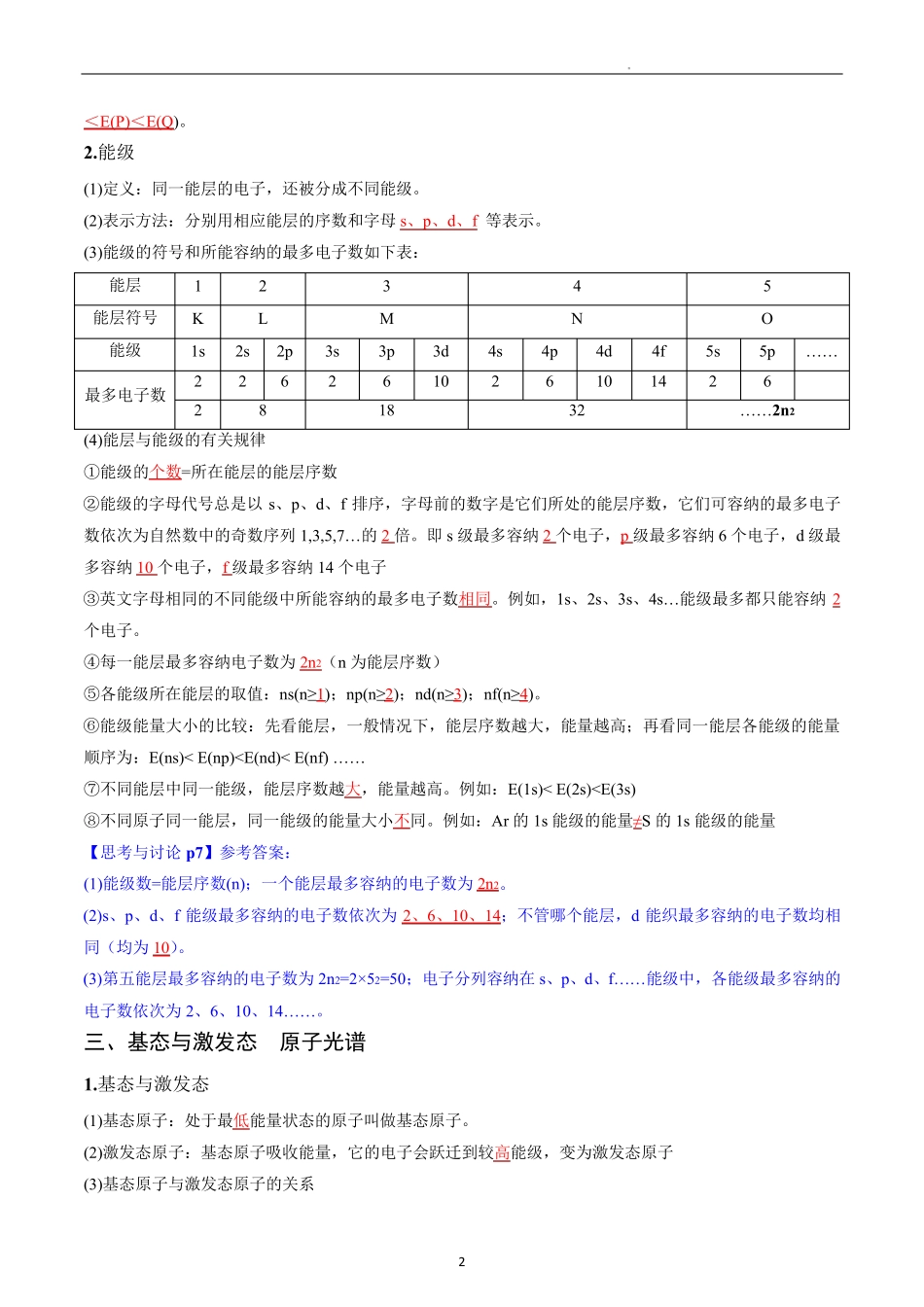
(3)能级的符号和所能容纳的最多电子数如下表: 能层 1 2 3 4 5 能层符号 K L M N O 能级 1s