化学物质结构与性质1. 铁及其氧化物是日常生活、生产中应用广泛的材料
请回答下列问题:(1) 基态铁原子的价电子轨道示意图为____________
(2) 铁元素常见的离子有Fe2+和 Fe3+,稳定性 Fe2+______Fe3+( 填“大于”或“小于”) ,原因是 ______________
(3) 纳米氧化铁能催化火箭推进剂NH4ClO4 的分解, NH+4 的结构式为 ________( 标出配位键) ,空间构型为 ________,其中氮原子的杂化方式为____________;与 ClO-4 互为等电子体的分子或离子有_________( 任写两种 )
(4) 金属铁晶体原子采用_____堆积
铁晶体的空间利用率为________( 用含 π 的式子表示)
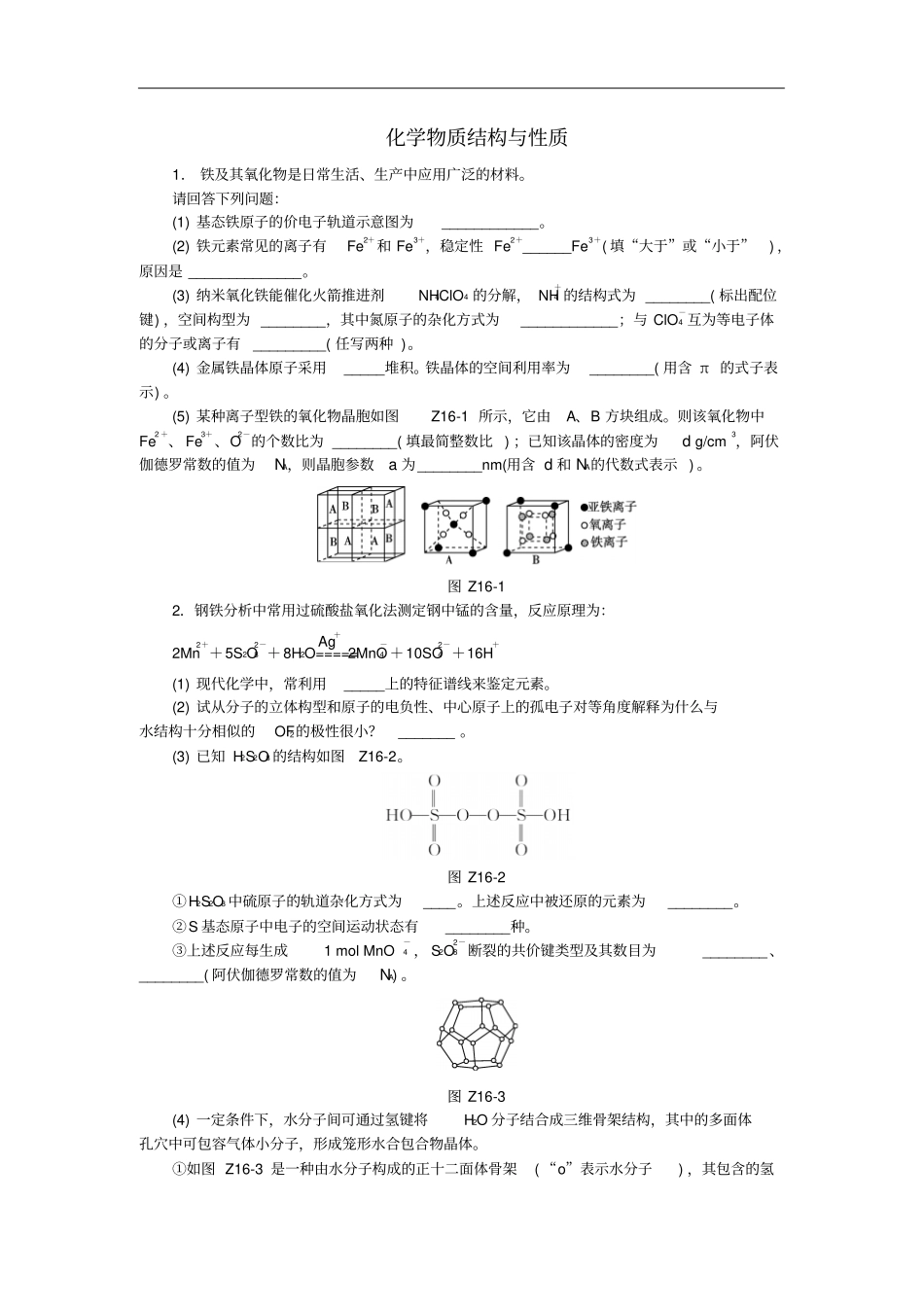
(5) 某种离子型铁的氧化物晶胞如图Z16-1 所示,它由A、B 方块组成
则该氧化物中Fe2 +、 Fe3+、O2-的个数比为 ________( 填最简整数比 ) ;已知该晶体的密度为d g/cm3,阿伏伽德罗常数的值为NA,则晶胞参数a 为________nm(用含 d 和 NA的代数式表示 )
图 Z16-12.钢铁分析中常用过硫酸盐氧化法测定钢中锰的含量,反应原理为:2Mn2++5S2O2-8 +8H2O=====Ag+2MnO-4 +10SO2-4 +16H+(1) 现代化学中,常利用_____上的特征谱线来鉴定元素
(2) 试从分子的立体构型和原子的电负性、中心原子上的孤电子对等角度解释为什么与水结构十分相似的OF2的极性很小
_______
(3) 已知 H2S2O8 的结构如图Z16-2
图 Z16-2①H2S2O8 中硫原子的轨道杂化方式为____
上述反应中被还原的元素为________
②S 基态原子中电子的空间运动状态有________种
③上述反应每生成1 mol Mn