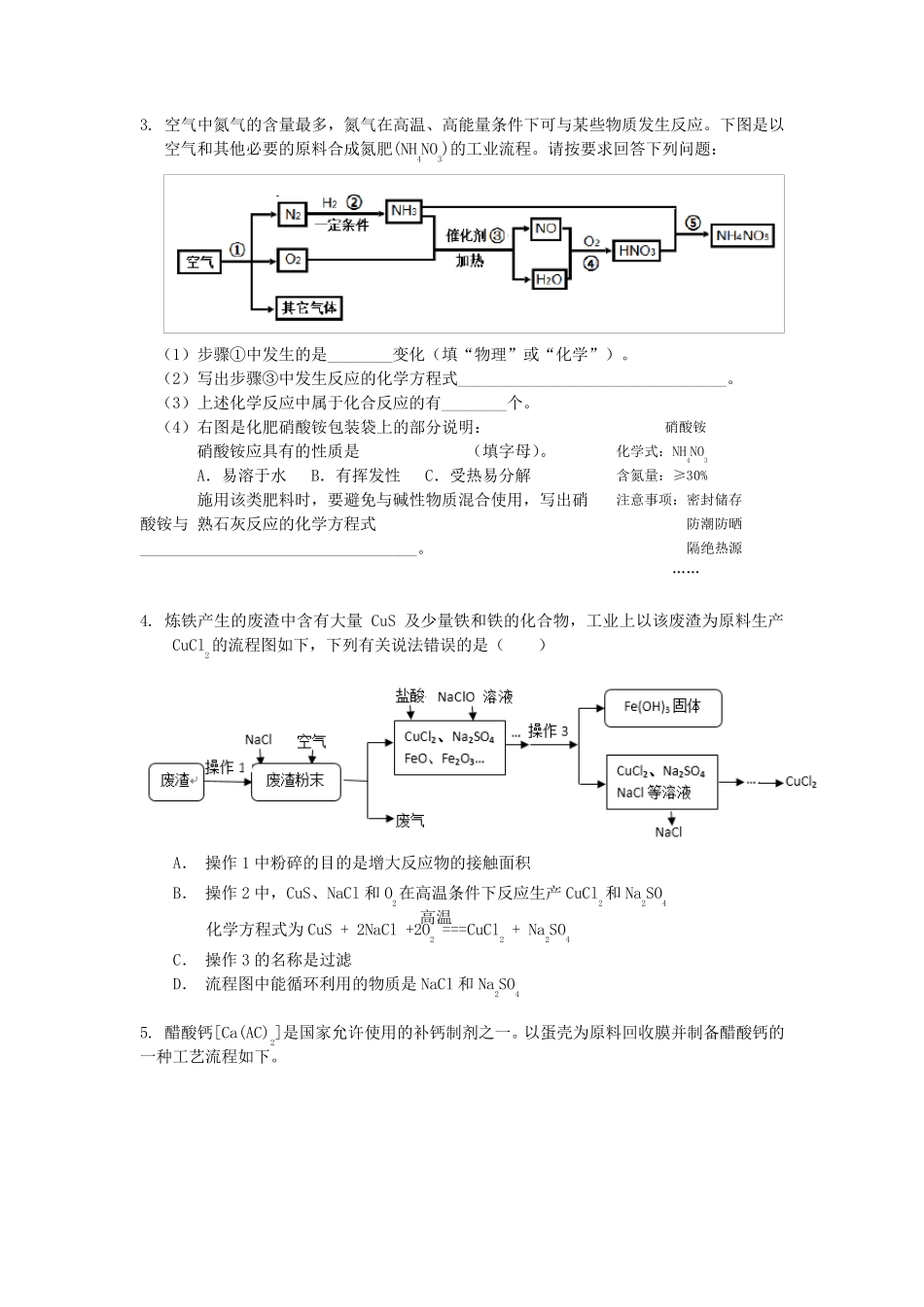
化学工艺流程图专题(1) 1.我国制碱工业先驱侯德榜发明了“侯氏制碱法”。其模拟流程如下: (1)反应①的化学方程式________________,反应②的基本反应类型为_______。 (2)工业上用分离液态空气 的方法制取氢气,属于_______变化(填“物理”或“化学”)。(3)操作a 的名称是_____,实验室进行此操作所需的玻璃仪器有烧杯、玻璃棒、______。 (4)写出NH4Cl 的一种用途________________。 2. 过氧化钙晶体﹝CaO2·8H2O﹞较稳定,呈白色,微溶于水,广泛应用于环境杀菌、消毒。以贝壳为原料制备 CaO2流程如下: (1)气体X 是CO2,其名称是 ;将过氧化钙晶体与溶液分离的方法是 。 (2)反应Y 需控制温度在0~5℃,可将反应容器放在 中,该反应是化合反应,反应产物是CaO2·8H2O,请写出化学方程式 。获得的过氧化钙晶体中常含有Ca(OH)2杂质,原因是 。 (3)CaO2的相对分子质量为 ,过氧化钙晶体﹝CaO2·8H2O﹞中H、O 元素的质量比为 。 (4)为测定制得的过氧化钙晶体中CaO2·8H2O 的质量分数,设计的实验如下:称取晶体样品50g,加热 到220℃充 分反应(方程式为2CaO2·8H2O=====△ 2CaO+ O2↑ + 16H2O↑ ,杂质不发生 变化),测得生 成 氧气的质量为3.2g,请计算 样品中CaO2·8H2O 的质量分数(CaO2·8H2O相对分子质量为216),写出必 要 的计算 过程。 高温 3. 空气中氮气的含量最多,氮气在高温、高能量条件下可与某些物质发生反应。下图是以空气和其他必要的原料合成氮肥(NH4NO3)的工业流程。请按要求回答下列问题: (1)步骤①中发生的是________变化(填“物理”或“化学”)。 (2)写出步骤③中发生反应的化学方程式_________________________________。 (3)上述化学反应中属于化合反应的有________个。 (4)右图是化肥硝酸铵包装袋上的部分说明: 硝酸铵应具有的性质是 (填字母)。 A.易溶于水 B.有挥发性 C.受热易分解 施用该类肥料时,要避免与碱性物质混合使用,写出硝酸铵与 熟石灰反应的化学方程式__________________________________。 4. 炼铁产生的废渣中含有大量CuS 及少量铁和铁的化合物,工业上以该废渣为原料生产CuCl2的流程图如下,下列有关说法错误的是( ) A. 操作1 中粉碎的目的是增大反应物的接触面积 B. 操作2 中,CuS、NaCl 和O2在高温条件下反应生产 CuCl2和Na2SO4 化学方程式为 CuS + 2NaCl +2O2 ===CuCl2 + Na2SO4 C....